题目内容
【题目】下列关于有机物的说法正确的是
A. 糖类、油脂、蛋白质在一定条件下均能水解
B. 乙二醇、苯乙烯在一定条件下均可聚合生成高分子化合物
C. 分子式为C4H8C12的有机物共有(不含立体异构)8种
D. ![]() 处于同一平面上的原子数最多为18个
处于同一平面上的原子数最多为18个
【答案】B
【解析】A.油脂、蛋白质在一定条件下均能水解,但糖类中的单糖如葡萄糖不水解,故A错误;B.乙二醇可通过缩聚生成高分子化合物,苯乙烯可通过加聚生成高分子化合物,故B正确;C.C4H8Cl2的同分异构体可以采取“定一移二”法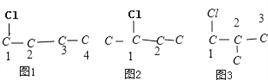 ,由图可知C4H8Cl2共有9种同分异构体,故C错误;D.该有机物中含有苯环、碳碳双键、碳碳三键、甲基,甲基中C原子处于乙烯和乙炔中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在乙烯或乙炔的平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子共平面,则两个甲基有2个氢原子可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故D错误;答案为B。
,由图可知C4H8Cl2共有9种同分异构体,故C错误;D.该有机物中含有苯环、碳碳双键、碳碳三键、甲基,甲基中C原子处于乙烯和乙炔中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在乙烯或乙炔的平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子共平面,则两个甲基有2个氢原子可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故D错误;答案为B。

【题目】(1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
实验编号 | 实验温度/℃ | c(Na2S2O3)/mol·L-1 | V(Na2S2O3)/mL | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | V(H2O)/mL |
① | 25 | 0.1 | 5.0 | 0.1 | 10.0 | a |
② | 25 | 0.1 | 10.0 | 0.1 | 10.0 | 0 |
③ | 25 | 0.2 | 5.0 | 0.1 | 5.0 | b |
④ | 50 | 0.2 | 5.0 | 0.1 | 10.0 | 5.0 |
其他条件不变时:探究温度对化学反应速率的影响,应选择实验__________(填实验编号);若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中a和b分别为________和________。
(2)某同学设计如下实验流程探究Na2S2O3的化学性质。
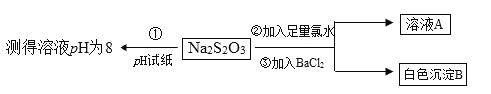
实验操作①中测试时pH试纸的颜色应该接近_____________。
A.红色 B.黄色 C.深蓝色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的_____性。
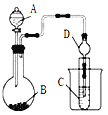
【题目】某学习小组通过下列装置探究MnO2与FeCl3·6H2O能否反应产生Cl2,FeCl3的升华温度为315℃。
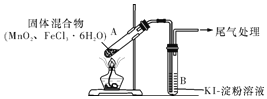
实验操作和现象:
操作 | 现象 |
点燃酒精灯,加热 | ⅰ.A中部分固体溶解,上方出现白雾 ⅱ.稍后,产生黄色气体,管壁附着黄色液滴 ⅲ.B中溶液变蓝 |
(1)现象ⅰ中的白雾是___。
(2)分析现象ⅱ,该小组探究黄色气体的成分,实验如下:
a.加热FeCl3·6H2O,产生白雾和黄色气体。
b.用KSCN溶液检验现象ⅱ和a中的黄色气体,溶液均变红。通过该实验说明现象ⅱ中黄色气体含有___。
(3)除了氯气可使B中溶液变蓝外,推测还可能的原因是:
①实验b检出的气体使之变蓝,反应的离子方程式是___。经实验证实推测成立。
②溶液变蓝的另外一种原因是:在酸性条件下,装置中的空气使之变蓝。通过进一步实验确认了这种可能性,其实验方案是___。
(4)为进一步确认黄色气体是否含有Cl2,小组提出两种方案,均证实了Cl2的存在。
方案1:在A、B间增加盛有某种试剂的洗气瓶C。
方案2:将B中KI淀粉溶液替换为NaBr溶液;检验Fe2+。
现象如下:
方案1 | B中溶液变为蓝色 |
方案2 | B中溶液呈浅橙红色,未检出Fe2+ |
①方案1的C中盛放的试剂是___(填字母)。
A.NaCl饱和溶液 B.NaOH溶液 C.NaClO溶液
②方案2中检验Fe2+的原因是___。
③综合方案1、2的现象,说明选择NaBr溶液的依据是___。
(5)将A中的产物分离得到Fe2O3和MnCl2,A中产生Cl2的化学方程式是:___。