题目内容
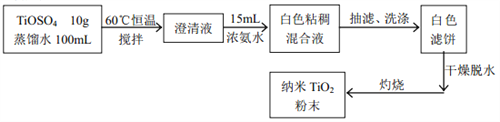
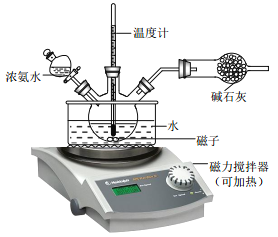
【题目】氨气是工农业生产中不可或缺的物质,研究制取氨气的机理意义非凡。
(1)在常温、常压、光照条件下,N2在掺有少量Fe2O3的TiO2催化剂表面与水发生下列反应:
N2(g)+3H2O(l)![]() 2NH3(g)+
2NH3(g)+![]() O2(g) △H="a" kJ mol-1。
O2(g) △H="a" kJ mol-1。
为进一步研究生成NH3的物质的量与温度的关系,常压下达到平衡时测得部分实验数据如下:
T/K | 303 | 313 | 323 |
n(NH3)/(l0-2mol) | 4.8 | 5.9 | 6.0 |
此反应的a_________0,△S________0。(填“>”“<”或“ = ”)
(2)—定温度和压强下,在2 L的恒容密闭容器中合成氨气:N2(g)+3H2(g)![]() 2NH3(g) △H="-92.4" kJ mol-1。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。
2NH3(g) △H="-92.4" kJ mol-1。在反应过程中反应物和生成物的物质的量随时间的变化如图所示。

① 0~10 min内,以NH3表示的平均反应速率为_________。
② 在10~20 min内,NH3浓度变化的原因可能是_______。
A.加入催化剂 B.缩小容器体积 C.降低温度 D.增加NH3的物质的量
③ 在反应进行至25 min时,曲线发生变化的原因是____________,达到第二次平衡时,新平衡的平衡常数K2______K1(填“>”“<”或“ = ”)
【答案】(1)> ;>
(2)①0.005 mol L-1 min-1
②BC
③移走 0.1 molNH3; =
【解析】试题分析:(1)升高温度NH3的物质的量最多,所以N2(g)+3H2O(l)![]() 2NH3(g)+
2NH3(g)+![]() O2反应吸热,a>0;反应后气体物质的量增多,△S>0;(2)① 0~10 min内,以NH3表示的平均反应速率为
O2反应吸热,a>0;反应后气体物质的量增多,△S>0;(2)① 0~10 min内,以NH3表示的平均反应速率为![]()
![]() 0.005 mol L-1 min-1;② 在10~20 min内,NH3浓度逐渐增大,变化的原因可能是A.加入催化剂,平衡不移动,NH3物质的量不变,A错误; B.缩小容器体积,平衡正向移动,氨气的物质的量增大,B正确 ; C.降低温度,平衡正向移动,NH3物质的量增大,C正确; D.增加NH3的物质的量,平衡逆向移动,氮气、氢气增多,D错误;③ 在反应进行至25 min时,氨气的物质的量突然由0.3mol变为0.2mol,曲线发生变化的原因是移走 0.1 molNH3,平衡常数只与温度有关,温度不变平衡常数不变,达到第二次平衡时,新平衡的平衡常数K2=K1。
0.005 mol L-1 min-1;② 在10~20 min内,NH3浓度逐渐增大,变化的原因可能是A.加入催化剂,平衡不移动,NH3物质的量不变,A错误; B.缩小容器体积,平衡正向移动,氨气的物质的量增大,B正确 ; C.降低温度,平衡正向移动,NH3物质的量增大,C正确; D.增加NH3的物质的量,平衡逆向移动,氮气、氢气增多,D错误;③ 在反应进行至25 min时,氨气的物质的量突然由0.3mol变为0.2mol,曲线发生变化的原因是移走 0.1 molNH3,平衡常数只与温度有关,温度不变平衡常数不变,达到第二次平衡时,新平衡的平衡常数K2=K1。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某研究性学习小组用浓度为0.20mol·L-1的盐酸标准液滴定含有一定量杂质的烧碱样品(杂质与酸不反应)溶于水形成的溶液。

(1)准确量取一定体积的待测液需要使用的仪器是______________。
(2)若滴定开始和结束时,滴定管中的液面如图所示,则消耗盐酸标准液的体积为________mL。
(3)滴定时,若以酚酞为指示剂,滴定达到终点的标志是______________________________。
(4)将准确称取的5.0g烧碱样品配制成250mL待测液,并用盐酸标准液滴定。滴定前读数及滴定后读数如下表所示。
滴定次数 | 待测液体积(mL) | 0.20mol·L-1的盐酸体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 10.00 | 0.70 | 20. 60 |
第一次 | 10.00 | 4.00 | 24.10 |
第三次 | 10.00 | 1.10 | 21.10 |
由实验数据可知,烧碱的纯度为__________。
(5)下列操作会导致测得的待测液的浓度偏大的是________(填字母)。
a.部分标准液滴出锥形瓶外 b.用待测溶液润洗锥形瓶
C.锥形瓶洗净后还留有蒸馏水 d.放出碱液的滴定管开始有气泡,放出液体后气泡消失