题目内容
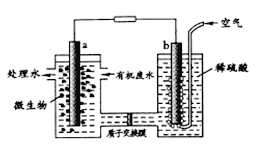
【题目】二氯化碳利用具有十分重要的意义,科学家有以下几个设想。
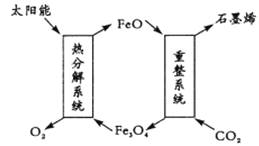
(1)用太阳能将CO2转化成O2和C(石墨烯),其设想如下:
①Fe3O4中Fe的化合价是+ 2和 __________;
②重整系统发生反应的化学方程式为______________________________。
(2)二氧化碳和氢气在催化剂作用下可制取低碳烯烃。在一密闭容器中分别投入1molCO2、3molH2,发生反应:2CO2(g)+6H2(g)![]() C2H4 (g)+ 4H2O(g) △H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如右下图所示。
C2H4 (g)+ 4H2O(g) △H;在不同温度下,用传感技术测出平衡时H2的物质的量变化关系如右下图所示。
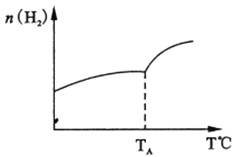
① 其它条件不变,起始时若按lmolCO2、2molH2进行投料,CO2转化率将_____________(填“增大”、“ 减小”或“不变”);
②△H________0(填“>”“<”“ 不能确定”)。
③若测试中体系内无氧气产生,试结合图示推断热稳定性C2H4 ________ H2O (填“>”“<”“ 不能确定”)。
(3)用氨水吸收CO2制化肥(NH4HCO3)
①已知:NH3·H2O(aq) ![]() NH4+ (aq) +OH-(aq) △H1=a kJmol-1
NH4+ (aq) +OH-(aq) △H1=a kJmol-1
CO2 (g) + H2O(l)![]() H2CO3 (aq) △H2=bkJmol-1
H2CO3 (aq) △H2=bkJmol-1
H2CO3(aq) + OH-(aq)![]() HCO3-(aq) + H2O(l) △H3=ckJmol-1
HCO3-(aq) + H2O(l) △H3=ckJmol-1
则利用NH3 H2O吸收CO2制备NH4HCO3的热化学方程式为_____________________________;
②已知常温下相关数据如表:
Kb(NH3·H2O) | 2×10-5mol L-1 |
Ka1(H2CO3) | 4×10-7mol L-1 |
Ka2(H2CO3) | 4×10-11mol L-1 |
则反应NH4++HCO3-+H2O![]() NH3 H2O+ H2CO3的平衡常数k=___________。
NH3 H2O+ H2CO3的平衡常数k=___________。
【答案】 +3 6FeO+CO2==2Fe3O4+C 减小 < < NH3·H2O(aq)+CO2(g)![]() NH4+ (aq)+ HCO3-(aq) △H=(a+b+c) kJmol-1 1.25×10-3
NH4+ (aq)+ HCO3-(aq) △H=(a+b+c) kJmol-1 1.25×10-3
【解析】(1)①本题考查四氧化三铁中铁的价态,四氧化三铁中铁元素以+2价、+3价;②根据原理,重整系统中加入FeO和CO2,生成石墨烯和Fe3O4,因此反应方程式为6FeO+CO2=2Fe3O4+C;(2)本题考查影响化学反应平衡移动的因素,①现在通入1molCO2和2molH2,相当于在原来的基础上减少氢气的量,平衡向逆反应方向进行,CO2的转化率减小;②随着温度的升高,氢气的物质的量增大,说明反应向逆反应方向进行,根据勒夏特列原理,正反应方向是放热反应,即△H<0;③根据图示,如果乙烯的稳定性大于水,则会产生氧气,但现在体系中没有氧气产生,因此C2H4的稳定性小于H2O;(3)①本题考查热化学反应方程式的计算,NH3·H2O(aq) ![]() NH4+ (aq) +OH-(aq) ①,CO2 (g) + H2O(l)
NH4+ (aq) +OH-(aq) ①,CO2 (g) + H2O(l)![]() H2CO3 (aq)②,H2CO3(aq) + OH-(aq)
H2CO3 (aq)②,H2CO3(aq) + OH-(aq)![]() HCO3-(aq) + H2O(l)③,NH3·H2O与CO2反应生成NH4HCO3的反应是NH3·H2O+CO2=NH4HCO3,因此是①+②+③得出NH3·H2O(aq)+CO2(g)
HCO3-(aq) + H2O(l)③,NH3·H2O与CO2反应生成NH4HCO3的反应是NH3·H2O+CO2=NH4HCO3,因此是①+②+③得出NH3·H2O(aq)+CO2(g)![]() NH4+ (aq)+ HCO3-(aq) △H=(a+b+c) kJmol-1;②根据反应,平衡常数K=c(H2CO3)×c(NH3·H2O)/[c(NH4+)×c(HCO3-)],分子分母同乘以c(H+)×c(OH-),得出:K=Kw/(Ka1(H2CO3)×Kb(NH3·H2O)=1.25×10-3。
NH4+ (aq)+ HCO3-(aq) △H=(a+b+c) kJmol-1;②根据反应,平衡常数K=c(H2CO3)×c(NH3·H2O)/[c(NH4+)×c(HCO3-)],分子分母同乘以c(H+)×c(OH-),得出:K=Kw/(Ka1(H2CO3)×Kb(NH3·H2O)=1.25×10-3。

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案【题目】工业燃烧煤、石油等化石燃料释放出大量NOx、CO、CO2等气体,严重污染空气,对废气进行脱硝,脱碳等处理可实现绿色环保、废物利用。
Ⅰ、脱硝:
已知:①H2的热值为142.9kJ/g(热值是表示单位质量的燃料完全燃烧生成稳定的化合物时所放出的热量);
②N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ/mol
③H2O(g)=H2O(l) ΔH=-44kJ/mol
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:_______
Ⅱ、脱碳
(1)CO与空气可设计成燃料电池(以熔融的碳酸盐为电解质)。写出该电池的负极反应式:_______。
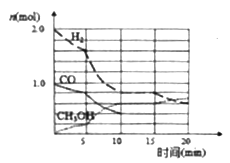
(2)甲醇是一种可再生能源,工业上可用合成气制备甲醇,反应为CO(g)+2H2(g) ![]() CH3OH(g)。某温度下在容积为VL的密闭容器中进行反应,其相关数据戔右图;反应开始至平衡时,用H2表示化学反应速率为________。该温度下CO的平衡转化率为_________。
CH3OH(g)。某温度下在容积为VL的密闭容器中进行反应,其相关数据戔右图;反应开始至平衡时,用H2表示化学反应速率为________。该温度下CO的平衡转化率为_________。
(3)向1L密闭容器中加入1molCO2、3molH2,在适当的条件下,发生反应CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g).
CH3OH(g)+H2O(g).
①下列叙述能说明此反应达到平衡状态的是___________。
a.混合气体的平均相对分子质量保持不变
b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等
d.混合气体的密度保持不变
e.1molCO2生成的同时又3molH-H键断裂
②相同条件下,在容积都为1L且固定的两个密闭容器中,按如下方式加入反应物,一段时间后反应达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1mol CO2、3molH2 | amol CO2、3amolH2 bmolCH3OH(g)、bmolH2O(g) |
若甲中平衡后气体的压强为开始的0.6倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆向反应方向进行,则b的取值可能为_________(填序号)
a.0.7 b.0.9 c.1.2
若保持温度不变,起始加入0.5molCO2、0.5molH2、0.5molCH3OH(g)、0.5molH2O(g) 则此反应速率的关系:v正__________v逆。(填“>”、“<”或“=”)