��Ŀ����
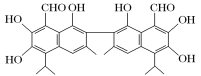
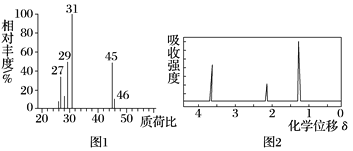
����Ŀ��ij�������A������ͼ��������Է�������Ϊ84��������ױ��������к���̼̼˫�����˴Ź������ױ���������ֻ��һ�����͵��⣮
��1��A�Ľṹ��ʽΪ_______________________��
��2��A�п϶������̼ԭ������__����
��3����0.1 mol����A��ȫȼ�պ�ȼ��ʱ���ı�״���µ�����____L��
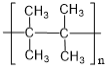
��4��A�ڴ������������·����Ӿ۷�Ӧ����ѧ����ʽΪ_______________________________��
��5���ڴ��������£���H2�ӳɺ�IJ�������Ϊ_____________________________��
���𰸡�![]() 6 20.16 n
6 20.16 n![]()
![]()
 2��3����������
2��3����������
��������
��1���������ķ���ʽ�ص㲢��Ϻ�����ױ��������к���̼̼˫�����˴Ź������ױ���������ֻ��һ�����͵�����з�����
��2�����ݻ�ѧ���������з����������⣻
��3�������������ȼ�շ���ʽCxHy+��x+y/4��O2![]() xCO2+y/2H2O��⣻
xCO2+y/2H2O��⣻
��4�����л����к���˫�������ݼӳɷ�Ӧ�ص���д���ɣ�
��5�����ݼӳɺ���л���Ϊ����������������
��1����������л���ΪCxHy����������Է�������Ϊ84��֪��12x+y=84��x��y��Ϊ���������������̼ԭ���ļ۹�����ã�x=6��y=12�����ݸ��л��������ױ��������к���̼̼˫�����˴Ź������ױ���������ֻ��һ�����͵����д����ṹ��ʽΪ��![]() ��
��
��2��![]() ���
�д���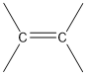 ���ɴ˿�֪��������6��̼ԭ��һ�����棻
���ɴ˿�֪��������6��̼ԭ��һ�����棻
��3��������������֪�������ķ���ʽΪC6H12����������������ȼ�շ���ʽΪ��C6H12+9O2![]() 6CO2+6H2O��֪��0.1mol��C6H12��ȫȼ�պ�ȼ��ʱ���ı�״���µ����������Ϊ��0.9mol��22.4L/mol=20.16L��
6CO2+6H2O��֪��0.1mol��C6H12��ȫȼ�պ�ȼ��ʱ���ı�״���µ����������Ϊ��0.9mol��22.4L/mol=20.16L��
��4��![]() �ڴ������������·����Ӿ۷�Ӧ����ѧ����ʽΪn
�ڴ������������·����Ӿ۷�Ӧ����ѧ����ʽΪn![]()
![]()
 ��
��
��5��![]() �ڴ��������£���H2�ӳɺ�IJ���Ϊ��
�ڴ��������£���H2�ӳɺ�IJ���Ϊ��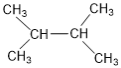 ��������ѡ���Լ����Ϊ��
��������ѡ���Լ����Ϊ��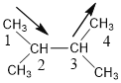 ��������Ϊ��2��3���������飻
��������Ϊ��2��3���������飻

 ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д� ��������ϵ�д�
��������ϵ�д�����Ŀ����2 L���ܱ������ڣ�500��ʱ��Ӧ2SO2(g)��O2(g) ![]() 2SO3(g)��H<0��ϵ�У�n(SO2)��ʱ��ı仯�����
2SO3(g)��H<0��ϵ�У�n(SO2)��ʱ��ı仯�����
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)д���÷�Ӧ��ƽ�ⳣ������ʽ��K��______________________��
(2)��ͼ��ʾSO3�ı仯��������__________����O2��ʾ��0��2s�ڸ÷�Ӧ��ƽ������v��______________��

(3)��˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(SO3)��2v(O2) b��������ѹǿ���ֲ���
c��v��(SO2)��2v��(O2) d���������ܶȱ��ֲ���
(4)Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����________��
a����ʱ�����SO3���� b���ʵ������¶� c������O2��Ũ�� d��ѡ���Ч����
(5)�����ݻ���Ϊ2 L���ܱ������ڣ�500��ʱ����ͬ��ʽͶ�뷴Ӧ�������Ӧ2SO2(g)��O2(g)![]() 2SO3(g)��H=-QkJ��mol-1(Q>0)�����ֺ��º��ݡ���ʼͶ����������ﵽƽ��ʱ���й���������:
2SO3(g)��H=-QkJ��mol-1(Q>0)�����ֺ��º��ݡ���ʼͶ����������ﵽƽ��ʱ���й���������:
ʵ�� | �� | �� | �� |
��ʼͶ�� | 2molSO2�� 1molO2 | 2molSO3 | 4molSO2�� 2molO2 |
ƽ��ʱn(SO3) | 0.5mol | n2 | n3 |
��Ӧ�������仯 | �ų�Q1kJ | ����Q2kJ | �ų�Q3kJ |
��ϵ��ѹǿ | p1 | p2 | p3 |
��Ӧ���ת���� | ��1 | ��2 | ��3 |
���������еķ�Ӧ�ֱ��ƽ��ʱ���и������ݹ�ϵ��ȷ����____(����ĸ)��
A.��1+��2=1 B. Q1+Q2=Q C. ��3<��1 D. p3<2p1=2p2 E. n2<n3<1.0mol F. Q3=2Q1
(6)��һ�������½��з�Ӧ2SO2(g)��O2(g) ![]() 2SO3(g)����ͼ��ʾ��
2SO3(g)����ͼ��ʾ��
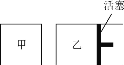
��ͬ�¶��£��ڼס����������и�Ͷ��2molSO2��1molO2���ס����������ij�ʼ�����Ϊ1L���ס��������ﵽƽ������ʱ�䣺��____(�>������<����=��,��ͬ)�ң�ƽ��ʱSO2��ת���ʣ���____�ҡ�