题目内容
【题目】用NA表示阿伏伽德罗常数.下列说法正确的是( )
A.标准状况下,22.4 L 苯中含有的苯分子数是NA
B.标准状况下,1mol氦气中含有的核外电子数为4NA
C.常温常压下,15g乙烷分子中含有的碳氢键数目为3 NA
D.常温常压下,0.10 molL﹣1CH3COOH溶液中含有的H+数小于0.1NA
【答案】C
【解析】A.标况下苯为液体,不能使用气体摩尔体积,故A不符合题意;
B.标准状况下,1mol氦气中含有的核外电子数为2NA,故B不符合题意;
C.15g乙烷的物质的量n= ![]() =0.5mol,而1mol乙烷中含6molC﹣H键,则0.5mol乙烷中含3mol碳氢键即3NA个,故C符合题意;
=0.5mol,而1mol乙烷中含6molC﹣H键,则0.5mol乙烷中含3mol碳氢键即3NA个,故C符合题意;
D.溶液体积未知,无法计算溶液中含有的氢离子数目,故D不符合题意;
所以答案是:C.

 阅读快车系列答案
阅读快车系列答案【题目】Ⅰ.在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(moll) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)下图中表示NO2的变化的曲线是___________(填字母);
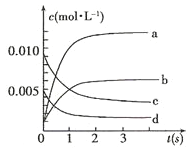
(2)800℃,反应达到平衡时,NO的转化率是___________;
(3)用O2表示从0~2s内该反应的平均速率v=___________。
Ⅱ.将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
(1)下列不能判断该分解反应已经达到化学平衡状态的是___________(填选项);
A.2v生(NH3)=v耗(CO2) B.密闭容器中氨气的物质的量不变
C.容器中CO2与NH3的物质的量之比保持不变 D.密闭容器中总压强保持不变
E.形成6个N-H键的同时有2个C=O键断裂
(2)能使该反应的反应速率增大的是___________(填选项);
A.及时分离出CO2气体 B.适当升高温度
C.加入少量NH2COONH4(s) D.选择高效催化剂
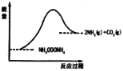
(3)如图所示,上述反应中断开反应物中化学键吸收的能量___________形成生成物中化学键放出的能量(填写“大于”“等于”“小于”)。
【题目】下列物质的分类正确的是
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | HCl | NaOH | SO2 | CO2 |
B | NaOH | H2SO4 | NaCl | Na2O | CO2 |
C | KOH | HNO3 | CaCO3 | CaO | CO |
D | NaOH | HCl | CaF2 | Na2O2 | SO2 |
A.AB.BC.CD.D


