题目内容
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2OA.正极反应式为:O2+2H2O+4e-![]() 4OH-
4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.以网状的铂为正极,可增大与氧气的接触面积
D.该电池通常只需要换铝板就可以继续使用
解析:从电池总反应式可以看出,铝失电子为负极材料,其反应式为Al-3e-![]() Al3+,而O2参与正极反应,其电极反应式为O2+2H2O+4e-
Al3+,而O2参与正极反应,其电极反应式为O2+2H2O+4e-![]() 4OH-;因此该电池工作时电子应由铝沿导线流向铂电极,故A项正确,B项错误,网状铂可以增大与O2的接触面积,C项正确;因Al参与反应被溶解需更换,而O2来自于空气无需考虑,所以D项正确。
4OH-;因此该电池工作时电子应由铝沿导线流向铂电极,故A项正确,B项错误,网状铂可以增大与O2的接触面积,C项正确;因Al参与反应被溶解需更换,而O2来自于空气无需考虑,所以D项正确。
答案:B

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
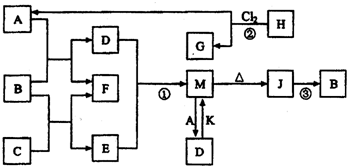 (1)C中存在的化学键类型为
(1)C中存在的化学键类型为