题目内容
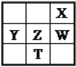
【题目】短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是
A.原子半径由小到大的顺序为![]()
B.X的简单氢化物的热稳定性比W的强
C.化合物YX、![]() 、
、![]() 中化学键的类型相同
中化学键的类型相同
D.W的最高价氧化物对应水化物的酸性比Z的弱
【答案】B
【解析】
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,故X原子有2个电子层,最外层电子数为6,故X为O元素,W与X属于同一主族,故W为S元素,Y原子的最外层只有2个电子,处于第ⅡA族,原子序数大于O元素,故Y为Mg元素,Z的单质常作为半导体材料,Z是Si元素。
A项、同主族元素自上而下,原子半径依次增大,故原子半径O<S,同周期元素自左而右,原子半径依次减小,故原子半径Mg>Si>S,则原子半径由小到大的顺序为Mg>Si>S>O,即X<W<Z<Y,故A错误;
B项、元素非金属性越强,简单氢化物的热稳定性越强,氧元素和硫元素为同主族元素,氧元素的非金属性强于硫元素,则氧元素的简单氢化物的热稳定性比硫元素的强,故B正确;
C项、氧化镁为离子化合物只含有离子键,二氧化硅和三氧化硫为共价化合物只含有共价键,化学键的类型不同,故C错误;
D项、元素非金属性越强,最高价氧化物对应水化物的酸性越强,硫元素和硅元素为同周期元素,硫元素的非金属性强于硅元素,则硫元素的最高价氧化物对应水化物的酸性比Z元素的强,故D错误;
故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案【题目】Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g) H=+11 kJ·mol-1。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g) H=+11 kJ·mol-1。在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |

由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示。当改变条件,再次达到平衡时,下列有关叙述不正确的是( )
A.若升高温度到某一温度,再次达到平衡时,相应点可能分别是A、E
B.若改变的条件是增大压强,再次达到平衡时,相应点与改变条件前相同
C.若改变的条件是使用催化剂,再次达到平衡时,相应点与改变条件前不同
D.若再次充入a mol HI,则达到平衡时,相应点的横坐标值不变,纵坐标值增大