题目内容
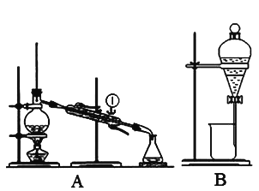
【题目】在25℃、101kPa条件下,将15L O2通往10L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气体中,V(CO)=__________L,V(H2)=___________L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气中,V(CO): V(H2)=_______。
(3)若剩余气体的体积为a L,则a的取值范围是_________
【答案】5 5 ![]() 10<a<20
10<a<20
【解析】
(1)设V(CO)为xL,则V(H2)为(10-x)L,
由2CO+O2=2CO2,△V
2 1 2 1
x ![]()
2H2 + O2=2H2O,△V
2 1 3
(10-x) ![]() (10-x)则
(10-x)则![]() +
+![]() (10-x)=15+10-15,解得x=5,即V(CO)=5L,则V(H2)=10L-5L=5L,故答案为:5;5;
(10-x)=15+10-15,解得x=5,即V(CO)=5L,则V(H2)=10L-5L=5L,故答案为:5;5;
(2)由(1)可得![]() +
+![]() (10-x)=15+10-a,解得x=(a-10)L,V(H2)=(10-x)L=(20-a)L,即V(CO):V(H2)=(a-10):(20-a),故答案为:(a-10):(20-a);
(10-x)=15+10-a,解得x=(a-10)L,V(H2)=(10-x)L=(20-a)L,即V(CO):V(H2)=(a-10):(20-a),故答案为:(a-10):(20-a);
(3)由(1)可得![]() +
+![]() (10-x)=15+10-a,解得:a=10+x,因0<x<10,则10<a<20,故答案为:10<a<20。
(10-x)=15+10-a,解得:a=10+x,因0<x<10,则10<a<20,故答案为:10<a<20。

 步步高达标卷系列答案
步步高达标卷系列答案【题目】实验室中有一未知浓度的稀盐酸,某学生在实验室中进行测定盐酸浓度的实验。请完成下列填空:
(1)配制500mL 0.1000mol·L-1 NaOH 标准溶液。
①配制所需的玻璃仪器有:烧杯、量筒、玻璃棒、__________、__________等。
②称取__________g氢氧化钠固体所需仪器有天平(带砝码、镊子)、药匙、__________
(2)取20.00 mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用__________(填仪器名称)盛装配制的标准NaOH溶液进行滴定。重复上述滴定操作23次,记录数据如下:
滴定次数 | 待测盐酸 的体积/mL | 标准NaOH溶液体积 | |
滴定前的刻度/mL | 滴定后的刻度/rnL | ||
第一次 | 20.00 | 0.40 | 20.50 |
第二次 | 20.00 | 4.10 | 24.00 |
第三次 | 20.00 | 1.00 | 24.00 |
(3)①如何判断滴定终点:____________________________。
②根据上述数据,可计算出该盐酸的浓度约为__________mol·L-1。
③排去碱式滴定管中气泡的方法应采用下图操作中的__________(填序号),然后轻轻挤压玻璃球使尖嘴部分充满碱液。

(4)在上述实验中,下列操作(其他操作正确)会造成测定果偏低的有__________(填序号)。
A.酸式滴定管使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体中混有Na2CO3固体
D.滴定终点读数时俯视读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失