题目内容
【题目】写出下列反应的热化学方程式.
(1)25℃,1.01×105Pa下,1g 硫粉在氧气中充分燃烧放出 9.36kJ热量,写出表示硫燃烧生成1molSO2的热化学方程式
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知: Cu(s)+2H+(aq)=Cu2+(aq)+H2(g)△H=+64.39kJ/mol
2H2O2(l)=2H2O(l)+O2(g)△H=﹣196.46kJ/mol
H2(g)+1/2O2(g)=H2O(l)△H=﹣285.84kJ/mol 在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 .
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是(填序号) 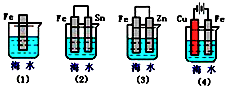
【答案】
(1)S(s)+O2(g)=SO2(g)△H=﹣299.52 kJ?mol﹣1
(2)Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=﹣319.6KJ/mol
(3)④②①③
【解析】解:(1)质量换算物质的量结合反应热计算得到生成1mol二氧化硫气体的焓变,1g 硫粉在氧气中充分燃烧放出 9.36kJ热量,生成1molSO2的反应放出的热量=9.36KJ×32=299.52 kJ;依据热化学方程式书写方法,标注物质聚集状态,和对应量的反应热;热化学方程式为:S(s)+O2(g)=SO2(g)△H=﹣299.52 kJmol﹣1;
所以答案是:S(s)+O2(g)=SO2(g)△H=﹣299.52 kJmol﹣1;(2)①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g)△H=+64.39kJ/mol
②2H2O2(l)=2H2O(l)+O2(g)△H=﹣196.46kJ/mol
③H2(g)+1/2O2(g)=H2O(l)△H=﹣285.84kJ/mol
依据盖斯定律①+ ![]() ②+③得到:Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=﹣319.6KJ/mol;
②+③得到:Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=﹣319.6KJ/mol;
所以答案是:Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=﹣319.6KJ/mol;(3)①是铁的化学腐蚀;②是原电池反应铁做负极被腐蚀;③形成原电池反应,铁做正极被保护;④电解池反应,铁做阳极被腐蚀;电解池阳极腐蚀最快,其次是原电池的负极,原电池正极被保护,所以Fe片腐蚀由快到慢的顺序是④②①③;
所以答案是:④②①③;
【考点精析】本题主要考查了金属的电化学腐蚀与防护的相关知识点,需要掌握金属的保护:涂保护层;保持干燥;改变金属的内部结构,使其稳定;牺牲阳极的阴极保护法即用一种更为活泼的金属与要保护的金属构成原电池;外加电源法才能正确解答此题.

 备战中考寒假系列答案
备战中考寒假系列答案【题目】下列物质的性质与用途有关联的是
选项 | 性质 | 用途 |
A | H2能在O2中燃烧并放出大量的热 | H2用作洁净燃料 |
B | 硝酸能与苯发生取代反应 | 苯用作溶剂 |
C | 葡萄糖能与新制Cu(OH)2悬浊液反应 | 葡萄糖可用作甜味剂 |
D | 乙酸能与NaOH溶液反应 | 乙酸可用作调味剂 |
A. A B. B C. C D. D