题目内容
【题目】学校实验室新购买了高锰酸钾试剂,按分类应将它放在( )
药品柜 | 甲 | 乙 | 丙 | 丁 |
药品 | 氧化物 | 盐 | 酸 | 碱 |
A.甲柜
B.乙柜
C.丙柜
D.丁柜
【答案】B
【解析】解:高锰酸钾是由钾离子和高锰酸根离子组成的化合物,属于盐.故选:B.
【考点精析】通过灵活运用常见的氧化物、酸、碱和盐的判别,掌握酸的通性:有腐蚀性,溶液程酸性,能与活泼金属,碱,某些盐和金属氧化物反应;碱的通性:有腐蚀性,溶液程碱性,能与某些金属,酸,某些盐和非金属氧化物反应;盐的通性:有些盐有微弱的腐蚀性,溶液的酸碱度根据盐的性质判定;氧化物即可以解答此题.

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g) + 4NH3(g) ![]() 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。
①能说明该反应已达到平衡状态的标志是_______
a.反应速率![]() ( NH3) =
( NH3) =![]() ( N2)
( N2)
b.容器内压强不再随时间而发生变化
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
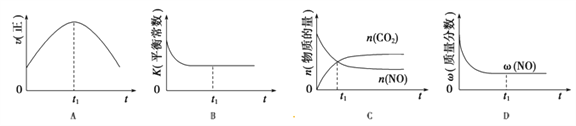
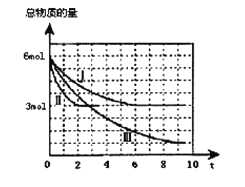
②某次实验中测得容器内NO及N2的物质的量随时间变化如图所示,图中b点对应的速率关系是![]() (正)____
(正)____![]() (逆)(填“﹥”、“﹤”或“﹦”),d点对应的速率关系是
(逆)(填“﹥”、“﹤”或“﹦”),d点对应的速率关系是![]() (正)____
(正)____![]() (逆)(填﹥、﹤或﹦)。
(逆)(填﹥、﹤或﹦)。

(2)298 K时,若已知生成标准状况下2.24 L NH3时放出热量为4.62 kJ。写出合成氨反应的热化学方程式_______。在该温度下,取1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量总小于92.4 kJ,其原因是________。
(3)一定条件下,在2 L密闭容器内,反应2NO2(g)![]() N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表: