题目内容
【题目】取含HCl和MgSO4的混合溶液1L,逐滴加入1molL﹣1的Ba(OH)2溶液,如图为产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)间的关系图,请回答下列问题:
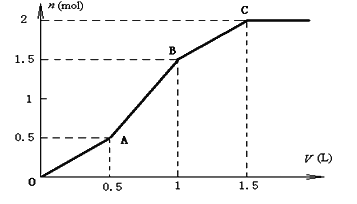
(1)OA段生成沉淀的化学式为______;
(2)AB段生成沉淀的离子方程式为:______;
(3)原溶液中的c(HCl)=______molL﹣1.
【答案】BaSO4 Ba2++SO42﹣=BaSO4↓、Mg2++2OH﹣=Mg(OH)2↓ 1
【解析】
含HCl和MgSO4的混合溶液中加入Ba(OH)2后,首先发生反应Ba2++SO42﹣=BaSO4↓,生成既不溶于水又不溶于酸的BaSO4沉淀,同时OH﹣跟H+发生中和反应:OH﹣+H+=H2O,OA段生成沉淀为BaSO4,HCl反应完毕,该阶段消耗n[Ba(OH)2]=0.5L×1mol/L=0.5mol,则n(HCl)=2n[Ba(OH)2]=1mol;
AB短生成沉淀量大于OA段,说明OA段Mg2+未反应,SO42﹣部分反应,继续加入Ba(OH)2,发生反应Ba2++SO42﹣=BaSO4↓、Mg2++2OH﹣=Mg(OH)2↓;
BC段生成沉淀量小于AB段,说明AB段中Mg2+完全反应,SO42﹣有剩余,再继续加入Ba(OH)2溶液,发生反应Ba2++SO42﹣=BaSO4↓,沉淀的量继续增大。
含HCl和MgSO4的混合溶液中加入Ba(OH)2后,首先发生反应Ba2++SO42﹣=BaSO4↓,生成既不溶于水又不溶于酸的BaSO4沉淀,同时OH﹣跟H+发生中和反应:OH﹣+H+=H2O,OA段生成沉淀为BaSO4,HCl反应完毕,该阶段消耗n[Ba(OH)2]=0.5L×1mol/L=0.5mol,则n(HCl)=2n[Ba(OH)2]=1mol;
AB短生成沉淀量大于OA段,说明OA段Mg2+未反应,SO42﹣部分反应,继续加入Ba(OH)2,发生反应Ba2++SO42﹣=BaSO4↓、Mg2++2OH﹣=Mg(OH)2↓;
BC段生成沉淀量小于AB段,说明AB段中Mg2+完全反应,SO42﹣有剩余,再继续加入Ba(OH)2溶液,发生反应Ba2++SO42﹣=BaSO4↓,沉淀的量继续增大。
(1)由上述分析可知,OA段生成沉淀的化学式为BaSO4;
(2)由上述分析可知,AB段生成沉淀的离子方程式为:Ba2++SO42﹣=BaSO4↓、Mg2++2OH﹣=Mg(OH)2↓;
(3)原溶液中的c(HCl)=![]() =1molL﹣1。
=1molL﹣1。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案【题目】为提纯下列物质![]() 括号内物质为杂质
括号内物质为杂质![]() ,所选用的试剂和分离方法都正确的是( )
,所选用的试剂和分离方法都正确的是( )
选项 | 物质 | 除杂试剂 | 分离方法或操作 |
A | 乙醇 | 无水 | 充分反应后蒸馏 |
B | 苯 | NaOH溶液 | 振荡静置后过滤 |
C | NaCl固体 | 水 | 高温溶解、降温结晶 |
D |
| 饱和 | 充分浸泡后过滤 |
A.AB.BC.CD.D