题目内容
取A、B、C三种金属各0.1 mol,分别与足量的盐酸反应,在标准状况下,共生成6.72 L氢气。又知B、C所产生的氢气的体积比是2∶1,且两者产生氢气的体积之和跟A产生的氢气相等。则在氯化物中A元素的化合价为( )
A.+1 B.+2 C.+3 D.+4
A.+1 B.+2 C.+3 D.+4
C
产生气体的物质的量共6.72 L÷22.4 L·mol-1="0.3" mol,依题意0.1 mol A产生气体:0.3 mol×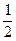 ="0.15" mol,即A与之产生的H2的物质的量之比为0.1∶0.15=2∶3,故A的化合价为+3。
="0.15" mol,即A与之产生的H2的物质的量之比为0.1∶0.15=2∶3,故A的化合价为+3。
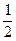 ="0.15" mol,即A与之产生的H2的物质的量之比为0.1∶0.15=2∶3,故A的化合价为+3。
="0.15" mol,即A与之产生的H2的物质的量之比为0.1∶0.15=2∶3,故A的化合价为+3。
练习册系列答案
相关题目
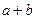
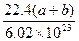
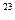
 ,则混合气体中NO与NO2的体积比为 …( )
,则混合气体中NO与NO2的体积比为 …( )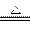 Cu3P2(s)+3H2,玻璃管质量增加4.96 g,第二支玻璃管中发生反应后质量减少了5.76 g。
Cu3P2(s)+3H2,玻璃管质量增加4.96 g,第二支玻璃管中发生反应后质量减少了5.76 g。