题目内容
【题目】下图所示是某化学兴趣小组根据教材知识设计的能说明Na2CO3与NaHCO3热稳定性的套管实验。下列叙述中不正确的是( )
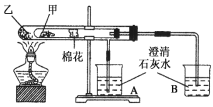
A. 甲为Na2CO3,乙为NaHCO3
B. 要证明NaHCO3受热能产生水,可在小试管内放置沾有少量无水硫酸铜粉末的棉花球
C. 加热不久就能看到B烧杯中的澄清石灰水变浑浊
D. 整个实验过程中A烧杯中的澄清石灰水无明显变化
【答案】A
【解析】
碳酸氢钠不稳定,受热易分解,生成Na2CO3、H2O、CO2,Na2CO3稳定,受热不分解。在套管实验中,内管应该放NaHCO3,外管放Na2CO3,Na2CO3直接受热,NaHCO3间接受热。B中的石灰水变浑浊,证明NaHCO3能在比较低的温度下分解。A中的石灰水始终不变浑浊,证明碳酸钠很稳定,即使直接受热也没有分解,从而证明了NaHCO3不稳定而Na2CO3稳定。
A.甲为NaHCO3,乙为Na2CO3,故A选;
B.无水硫酸铜遇水变成蓝色的CuSO4·5H2O,故B不选;
C.NaHCO3不稳定,受热分解产生的CO2进入B中,使石灰水变浑浊,故C不选;
D.Na2CO3稳定,受热不分解,所以A中的石灰水不会变浑浊,故D不选。
故选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目