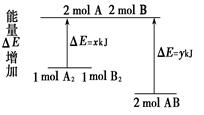
题目内容
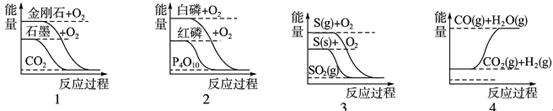
下列图像分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中正确的是(ΔH用于表示反应中的热量变化,ΔH>0表示反应吸热 ,ΔH<0 表示反应放热)

| A.石墨转变为金刚石是吸热反应 |
| B.白磷比红磷稳定 |
| C.S(g)+O2(g)===SO2(g) ΔH1S(s)+O2(g)===SO2(g) ΔH2则ΔH1>ΔH2 |
| D.CO(g)+H2O(g)===CO2(g)+H2(g) ΔH1>0 |
A
试题分析:根据图像可知,石墨的总能量低于金刚石的总能量,所以石墨转变为金刚石是吸热反应,A正确;白磷的总能量高于红磷的总能量,所以根据能量越低越稳定可知,红磷比白磷稳定性强,B不正确;气态S的总能量高于固态S的总能量,所以气态S燃烧放出的热量多,但放热越多反应热△H越小,所以C中ΔH2>ΔH1,C不正确;D中反应物的总能量高于生成物的总能量,反应是放热反应,D不正确,答案选A。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。该题的关键是明确影响反应热大小的因素,然后结合图像灵活运用即可。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 O2(g);△H="+765.2" kJ·mol-1,请在答题卡的坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注。
O2(g);△H="+765.2" kJ·mol-1,请在答题卡的坐标图中,画出上述反应过程中体系能量变化示意图,并进行必要标注。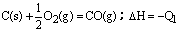 C(s) + O2(g)=CO2(g);△H=-Q2
C(s) + O2(g)=CO2(g);△H=-Q2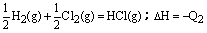
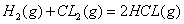 )在光照和点燃条件的△H相同
)在光照和点燃条件的△H相同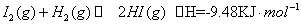
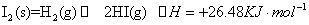
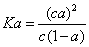 。若加入少量醋酸钠固体,则CH3COOH;—一CH3COO -十H+向左移动,a减小,Ka变小若加入少量醋酸钠固体,则
。若加入少量醋酸钠固体,则CH3COOH;—一CH3COO -十H+向左移动,a减小,Ka变小若加入少量醋酸钠固体,则
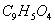 十H+向左移动,a减小,Ka变小
十H+向左移动,a减小,Ka变小