题目内容
对某弱酸稀溶液加热时,下列叙述中错误的是( )
| A、弱酸的电离程度增大 |
| B、弱酸分子的浓度减小 |
| C、溶液中c(H+)减小 |
| D、溶液的导电能力增强 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:加热弱酸稀溶液,促进弱酸电离,导致弱酸中氢离子和酸根离子浓度增大,溶液导电能力与离子浓度成正比,据此分析解答.
解答:
解:A.弱酸的电离是吸热反应,升高温度促进弱酸电离,弱酸的电离程度增大,故A正确;
B.升高温度促进弱酸电离,则弱酸分子浓度减小,故B正确;
C.升高温度促进弱酸电离,则氢离子浓度增大,故C错误;
D.升高温度促进弱酸电离,溶液中自由移动离子浓度增大,溶液的导电能力增强,故D正确;
故选C.
B.升高温度促进弱酸电离,则弱酸分子浓度减小,故B正确;
C.升高温度促进弱酸电离,则氢离子浓度增大,故C错误;
D.升高温度促进弱酸电离,溶液中自由移动离子浓度增大,溶液的导电能力增强,故D正确;
故选C.
点评:本题考查了弱电解质的电离,明确温度与弱电解质电离的关系即可解答,注意比较加水稀释和升高温度时溶液中离子浓度变化,题目难度不大,注意溶液导电能力与电解质强弱无关,为易错点.

练习册系列答案
相关题目
下列有关说法正确的是( )
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B、Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
| C、向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
将5.1g镁铝合金,投入500mL 2.0mol?L-1盐酸中,金属完全溶解,再加入4.0mol?L-1的NaOH溶液,若要生成的沉淀最多,则加入NaOH溶液的体积是( )
| A、200mL |
| B、425mL |
| C、250mL |
| D、560mL |
下列各组离子,在pH=0的溶液中可以大量共存的是( )
| A、Al3+、S2-、Br-、SO32- |
| B、Mg2+、Cu2+、SO42-、Br- |
| C、Na+、Fe2+、I-、MnO4- |
| D、NH4+、K+、HS-、Cl- |
同温同压下,下列各组热化学方程式中,△H1<△H2的是( )
| A、S(g)+O2(g)═SO2(g);△H1 S(s)+O2(g)═SO2(g);△H2 | ||||
B、
| ||||
| C、2H2(g)+O2(g)═2H2O(g);△H1 2H2(g)+O2(g)═2H2O(l);△H2 | ||||
D、C(s)+
|
下列离子方程式正确的是( )
| A、NaHCO3的水解:HCO3-+H2O═H3O++CO32- |
| B、向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
| C、1mol Cl2通入含1mol FeI2的溶液中:2Fe2++2I-+2Cl2═2Fe3++4Cl-+I2 |
| D、酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O═3I2+6OH- |
下列物质中互为同分异构体的是( )
| A、CH3CH2CH2CH3 |
B、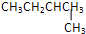 |
C、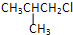 |
| D、CH3CH2CH2CH2Cl |
在下列反应中,硝酸既表现氧化性又表现酸性的是( )
| A、C和浓HNO3 |
| B、Al(OH)3和HNO3 |
| C、H2S和HNO3 |
| D、Fe3O4和HNO3 |
绿色化学对于化学反应提出了“原子经济性”的要求.理想的原子经济性反应是原料中的原子全部转化为产物,不产生副产品,实现零排放.下列几种生产乙苯的方法中,原子经济性最好的是( )
A、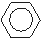 +C2H5Cl→ +C2H5Cl→ +HCl +HCl |
B、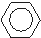 +C2H5OH→ +C2H5OH→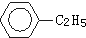 +H2O +H2O |
C、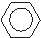 +CH2═CH2→ +CH2═CH2→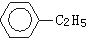 |
D、 +CH3CH3→ +CH3CH3→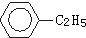 +HCl +HCl |