题目内容
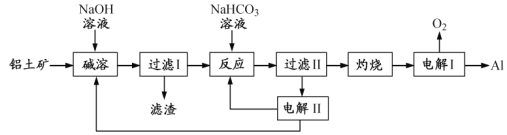
【题目】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:

请回答下列问题:
(1)本实验最适合的氧化剂X是___(填序号)。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)物质Y是____。
(3)本实验用加碱沉淀法能不能达到目的?___,原因是___。
(4)除去Fe3+的有关离子方程式是____。
(5)加氧化剂的目的是____。
(6)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体___,应如何操作___。
【答案】C CuO[或Cu(OH)2或CuCO3或Cu2(OH)2CO3] 不能 因加碱的同时也会使Cu2+生成Cu(OH)2沉淀 Fe3++3H2O![]() Fe(OH)3+3H+,CuO+2H+=Cu2++H2O[或Cu(OH)2+2H+=Cu2++2H2O等] 将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离 不能 应在HCl气流中加热蒸发
Fe(OH)3+3H+,CuO+2H+=Cu2++H2O[或Cu(OH)2+2H+=Cu2++2H2O等] 将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离 不能 应在HCl气流中加热蒸发
【解析】
加入氧化剂X的目的是把亚铁离子氧化,根据除杂原则,不能引入新的杂质;加入试剂Y的目的是调节pH使铁离子生成氢氧化铁沉淀,过滤除去沉淀,对滤液进行蒸发浓缩、冷却结晶、过滤得到氯化铜晶体;
(1)加入氧化剂,将Fe2+氧化为Fe3+,易除去,除杂时,不能引入新的杂质;
(2)物质Y的作用是调节溶液的pH,据此来选择合适的试剂;
(3)加碱的同时Cu2+也会生成沉淀;
(4)CuO能促进三价铁离子的水解;
(5)加入氧化剂,将Fe2+氧化为Fe3+;
(6) CuCl2属于强酸弱碱盐,加热蒸发时促进其水解(HCl易挥发)。
(1)根据题意,加入氧化剂X可把Fe2+氧化为Fe3+,而没有增加新杂质,所以X为H2O2;
故答案是:C;
(2)结合题示,调节pH至3.7,使Fe3+全部沉淀,所以Y最好为CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3] ;
故答案是: CuO[或Cu(OH)2或CuCO3或Cu2(OH)2CO3] ;
(3)加碱的同时,Cu2+也会生成沉淀;
答案是:不能;因加碱的同时也会使Cu2+生成Cu(OH)2沉淀;
(4)铁离子水解产生H+,氧化铜与H+ ,减小了氢离子浓度,促进了铁离子的水解,产生氢氧化铁沉淀,达到除去铁离子的目的;除去Fe3+的有关离子方程式:Fe3++3H2O![]() Fe(OH)3+3H+,CuO+2H+=Cu2++H2O[或Cu(OH)2+2H+=Cu2++2H2O等];
Fe(OH)3+3H+,CuO+2H+=Cu2++H2O[或Cu(OH)2+2H+=Cu2++2H2O等];
答案是: Fe3++3H2O![]() Fe(OH)3+3H+,CuO+2H+=Cu2++H2O[或Cu(OH)2+2H+=Cu2++2H2O等];
Fe(OH)3+3H+,CuO+2H+=Cu2++H2O[或Cu(OH)2+2H+=Cu2++2H2O等];
(5) Fe2+沉淀为氢氧化物时所需pH与Cu2+的沉淀的pH相同,也就是说, Fe2+沉淀的同时, Cu2+也会沉淀,无法将两者分离开,根据题干提供信息可以知道Fe3+沉淀所需的pH较小,所以应先将Fe2+氧化为Fe3+后再将其除去;
答案是: 将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离 ;
(6)CuCl2属于强酸弱碱盐,加热蒸发时促进其水解(HCl易挥发),所以应在HCl气氛中采用浓缩后冷却结晶的方法,以得到CuCl22H2O的晶体;
答案是: 不能;应在HCl气流中加热蒸发。

【题目】现有A、B、C、D、E五种均可溶于水的固体物质,是由以下提供的几种离子组成![]() 每种离子只能用一次
每种离子只能用一次![]() :
:
阳离子 |
|
阴离子 |
|
现分别进行如下实验:
![]() 将D与E的溶液混合加热,产生有刺激性气味的气体
将D与E的溶液混合加热,产生有刺激性气味的气体
![]() 将B与E的溶液混合,产生白色沉淀,向该沉淀中加入足量的稀硝酸,沉淀部分溶解
将B与E的溶液混合,产生白色沉淀,向该沉淀中加入足量的稀硝酸,沉淀部分溶解
![]() 在常温下用pH试纸测定溶液A的
在常温下用pH试纸测定溶液A的![]()
下列说法不正确的是![]()
A.物质E的化学式为![]() B.物质D中一定含有
B.物质D中一定含有![]()
C.难以确定物质A的组成D.物质C的化学式是![]()