题目内容
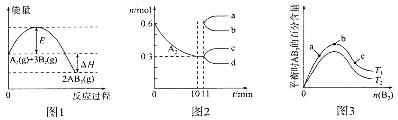
【题目】在一定条件下A2和B2可发生反应:A2(g)+3B2(g) ![]() 2AB3(g)。图1表示在一定温度下此反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时A2的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物B2的起始物质的量对此反应平衡的影响。下列说法错误的是
2AB3(g)。图1表示在一定温度下此反应过程中的能量变化,图2表示在固定容积为2L的密闭容器中反应时A2的物质的量随时间变化的关系,图3表示在其他条件不变的情况下,改变反应物B2的起始物质的量对此反应平衡的影响。下列说法错误的是
A. 该反应在低于某一温度时能自发进行
B. 10min内该反应的平均速率v(B2)=0.045mol/(L·min)
C. 11min时,其他条件不变,压缩容器容积至1L,n(A2)的变化趋势如图2中曲线d所示
D. 图3中T1<T2,b点对应状态下A2的转化率最高
【答案】D
【解析】
A.根据反应热及熵变判断体系的自由能分析;
B.根据v=![]() 及物质反应时速率比等于方程式中相应物质的化学计量数的比分析、判断;
及物质反应时速率比等于方程式中相应物质的化学计量数的比分析、判断;
C.根据缩小容器的容积,物质的浓度增大,平衡向气体体积减小的方向移动分析、判断;
D.利用浓度对化学平衡移动的影响分析判断。
A. 体系的自由能△G=△H-T△S,根据图示可知,该反应为放热反应,△H<0,由于该反应的正反应是气体体积减小的反应,所以△S<0。当温度较低时,△G=△H-T△S <0,反应能够自发进行;当温度较高时,T△S>△H,即△G>0,反应不能自发进行,A正确;
B.10min内该反应的平均速率v(A2)=![]() mol/(Lmin),根据方程式可知v(B2)=3v(A2)=0.045mol/(L·min),B正确;
mol/(Lmin),根据方程式可知v(B2)=3v(A2)=0.045mol/(L·min),B正确;
C.11min时,其他条件不变,压缩容器容积至1L,由于物质的浓度增大,化学平衡正向移动,不断消耗A2,所以n(A2)的物质的量会进一步减少,n(A2)变化趋势如图2中曲线d所示,C正确;
D.在温度不变时,增大某种反应物的浓度,化学平衡正向移动,可以使其它反应物的转化率提高,故当T1<T2,c点由于n(B2)最大,故其对应状态下A2的转化率最高,D错误;
故合理选项是D。