题目内容
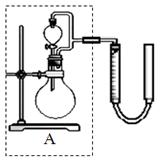
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )


A.反应的化学方程式:2M N N |
| B.t2时,正、逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时N的浓度是M浓度的2倍 |
D
试题分析:根据图像可知,反应进行到t2时M的我知道了增加了4mol-2mol=2mol,N的物质的量减少了8mol-4mol=4mol,所以该反应的化学方程式是N
 2M,A不正确。t2时,M和N的物质的量还是变化的,所以正、逆反应速率不相等,没有达到平衡状态,B不正确;t3时,M和N的物质的量不再变化,所以正、逆反应速率相等,达到平衡状态,C不正确;根据图像可知,选项D正确,答案选D。
2M,A不正确。t2时,M和N的物质的量还是变化的,所以正、逆反应速率不相等,没有达到平衡状态,B不正确;t3时,M和N的物质的量不再变化,所以正、逆反应速率相等,达到平衡状态,C不正确;根据图像可知,选项D正确,答案选D。点评:该题是中等难度的试题,试题贴近高考,在注重对学生基础知识巩固和检验的同时,侧重对学生能力的培养和方法的指导与训练,意在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确图像的变化特点,然后结合题意灵活运用即可。

练习册系列答案
相关题目


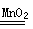 2H2O+O2↑可制备氧气。① 取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
2H2O+O2↑可制备氧气。① 取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。