题目内容
下列说法正确的是( )
| A、水加热到很高的温度都难以分解是因为水分子间存在氢键 |
| B、碳酸钠固体中不存在阴阳离子 |
| C、氢化锂三兄弟--LiH、LiD、LiT三种物质的质子数之比为4:5:6 |
D、乙醛分子的结构式为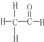 ,其一个分子中存在7对共用电子对 ,其一个分子中存在7对共用电子对 |
考点:含有氢键的物质,质量数与质子数、中子数之间的相互关系,不同晶体的结构微粒及微粒间作用力的区别,常见有机化合物的结构
专题:化学键与晶体结构
分析:A.H-O键的键能较大,故水加热到很高的温度都难以分解;
B.碳酸钠属于离子化合物;
C.H、D和T的质子数都为1;
D.乙醛分子的结构式为 ,4个碳氢单键、1个碳碳单键、1个碳氧双键,故存在7对共用电子对.
,4个碳氢单键、1个碳碳单键、1个碳氧双键,故存在7对共用电子对.
B.碳酸钠属于离子化合物;
C.H、D和T的质子数都为1;
D.乙醛分子的结构式为
 ,4个碳氢单键、1个碳碳单键、1个碳氧双键,故存在7对共用电子对.
,4个碳氢单键、1个碳碳单键、1个碳氧双键,故存在7对共用电子对.解答:
解:A.H-O键的键能较大,故水加热到很高的温度都难以分解,与氢键无关,故A错误;
B.碳酸钠属于离子化合物,存在阴阳离子,故B错误;
C.H、D和T的质子数都为1,故LiH、LiD、LiT三种物质的质子数之比为1:1:1,故C错误;
D.乙醛分子的结构式为 ,4个碳氢单键、1个碳碳单键、1个碳氧双键,故存在7对共用电子对,故D正确,
,4个碳氢单键、1个碳碳单键、1个碳氧双键,故存在7对共用电子对,故D正确,
故选D.
B.碳酸钠属于离子化合物,存在阴阳离子,故B错误;
C.H、D和T的质子数都为1,故LiH、LiD、LiT三种物质的质子数之比为1:1:1,故C错误;
D.乙醛分子的结构式为
 ,4个碳氢单键、1个碳碳单键、1个碳氧双键,故存在7对共用电子对,故D正确,
,4个碳氢单键、1个碳碳单键、1个碳氧双键,故存在7对共用电子对,故D正确,故选D.
点评:本题考查物质的性质与结构的关系,离子化合物的判断,有机物的结构,以及同位素的知识,难度不大.要注意平时基础知识的积累.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
下列说法正确的是( )
| A、浓硫酸溶于水的过程属于放热反应 |
| B、既有化学键断裂又有化学键生成的过程一定属于化学反应 |
| C、物质导电的过程一定是物理变化 |
| D、同分异构体之间的相互转化一定是化学变化 |
下列物质不能使红墨水褪色的是( )
| A、活性炭 | B、过氧化钠 |
| C、NaCl溶液 | D、漂白粉 |
下列化学变化中,能够一步实现的是( )
| A、Na→Na2O2 |
| B、Al2O3→Al(OH)3 |
| C、N2→HNO3 |
| D、S→SO3 |
现有X、Y两种VA族元素,下列事实不能说明X的非金属性比Y强的是( )
| A、两种元素所形成的气态氢化物的稳定性:XH3>YH3 |
| B、两种元素所形成的酸的酸性:H3XO4>H3YO4 |
| C、两种元素所形成的最高价氧化物的稳定性:X2O5>Y2O5 |
| D、两种元素形成气态氢化物的难易程度:X易于Y |
下列叙述正确的是( )
| A、乙烯、聚氯乙烯和苯分子中均含有碳碳双键 |
| B、淀粉、油脂、蛋白质都是天然高分子化合物且都能水解 |
| C、在蛋白质溶液中加入硫酸铜溶液,蛋白质会发生凝聚,加水后不能再溶解 |
| D、用氢氧化钠溶液,通过分液的方法,可以除去苯中的乙酸 |
下列物质中,不具有漂白作用的是( )
| A、SO2 |
| B、SiO2 |
| C、Na2O2 |
| D、Ca(ClO)2 |
物质丙的生产路线(反应条件略去)如图,下列叙述错误的是( )
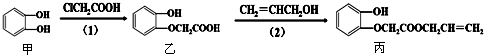
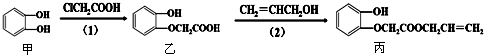
| A、步骤(1)产物中残留的物质甲可用FeCl3溶液检验 |
| B、物质甲和物质丙均可与酸性KMnO4溶液发生反应 |
| C、物质乙和物质丙均可与NaOH溶液发生反应 |
| D、步骤(2)产物中残留的丙烯醇不可用溴水检验 |
