题目内容
下列离子方程式中正确的是( )
| A.将SO2气体通入NaClO溶液中:SO2+2ClO-+H2O =SO32-+2HClO |
| B.向FeBr2溶液中通入过量Cl2:2Fe2++4Br-+2Cl2=2Fe3++2Br2+4Cl- |
| C.向硫酸氢钾溶液中加入Ba(OH)2溶液至中性:2H++SO42-+Ba2+ +2OH-= BaSO4↓+2H2O |
| D.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-= NH3↑+H2O |
C
解析试题分析:A.SO32-有还原性, HClO有氧化性,二者会继续发生氧化还原反应。反应的离子方程式为:
SO2 +ClO-+H2O =SO42-+2H++Cl-。错误。B.电荷不守恒。由于Cl2过量。所以向FeBr2溶液中通入过量Cl2反应的离子方程式为:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-.错误。C.符合客观事实及离子方程式的书写原则。正确。D.NH4HCO3电离产生的阳离子、阴离子都与OH-发生反应。反应的离子方程式为:NH4++ HCO3-+2OH- CO32-+NH3↑+2H2O.错误。
CO32-+NH3↑+2H2O.错误。
考点:考查离子方程式书写的知识。

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
甲、乙、丙是三种不含相同离子的可溶性电解质。它们所含的离子如下表所示:
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH—、NO3—、SO42— |
取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)>c(乙)>c(丙),下列说法错误的是
A.甲中一定含Na+ B.乙中一定含NH4+
C.丙中一定含Mg2+ D.丙中一定含SO42—
某无色透明的溶液,一定能大量共存的离子组是( )
| A.Cl-、SO42-、Na+、K+ | B.K+、CO32-、Ca2+、NO3- |
| C.HCO3-、Na+、NO3-、H+ | D.NO3-、Cu2+、Cl-、NH4+ |
下列化学方程式中,能用离子方程式:Ba2++SO42-=BaSO4↓表示的是
| A.Ba(OH)2+(NH4)2SO4=BaSO4↓+2NH3?H2O |
| B.Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C.BaCO3+H2SO4=BaSO4↓+2H2O+CO2↑ |
| D.BaCl2+ Na2SO4=BaSO4↓+2NaCl |
下列化学反应中,能用离子方程式 H+ + OH-== H2O 表示的是
A.2H2 + O2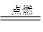 2H2O 2H2O |
| B.HCl + NaOH == NaCl + H2O |
| C.2HCl + Cu(OH)2== CuCl2 + 2H2O |
| D.Ba(OH)2 + H2SO4== BaSO4↓+ 2H2O |
在pH=1的无色溶液中,下列离子能大量共存的是
| A.NH4+、Ba2+、NO3—、CO32— | B.K+、Mg2+、NO3-、SO42— |
| C.Fe2+、OH—、SO42—、MnO4— | D.Na+、Fe3+、Cl—、AlO2— |
下列表示对应化学反应的离子方程式正确的是
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O | |
B.醋酸溶解鸡蛋壳:2H++CaCO3=Ca2++CO2↑+ H2O | C.NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ |
| D.向FeCl3溶液中加入Mg(OH)2: 3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
对下列图像的描述正确的是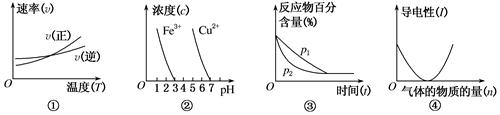
| A.根据图①可判断反应的ΔH <0 |
| B.根据图②,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
C.图③可表示压强(p)对反应2A(g)+2B(g)  3C(g)+D(s)的影响 3C(g)+D(s)的影响 |
| D.图④ 可表示向醋酸溶液中通入氨气时,溶液导电性随氨气量的变化 |