题目内容
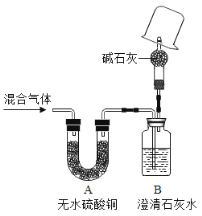
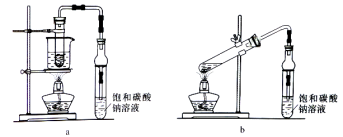
【题目】某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下:
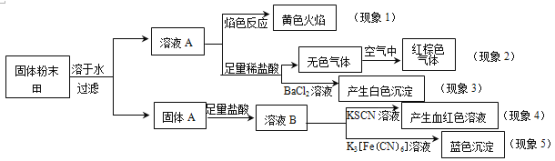
该同学得出的结论正确的是
A.根据现象1可推出该固体粉末中含有钠元素,但不含钾元素
B.根据现象2可推出该固体粉末中一定含有NaNO2
C.根据现象3可推出该固体粉末中一定含有Na2SO4
D.根据现象4和现象5可推出该固体粉末中一定含有FeO和Fe2O3
【答案】D
【解析】
试题分析:A.钠的焰色反应为黄色,所以一定含有钠元素,观察钾的焰色反应须透过蓝色钴玻璃,避免钠的干扰,无法确定是否含钾元素,A项错误;B.红棕色气体为NO2,则原混合物中可能含有硝酸钠或NaNO2或两者都存在,B项错误;C.K2SO3在酸性条件下发生氧化还原反应生成SO42-,加入氯化钡生成硫酸钡沉淀,则不一定含硫酸钠,可能有K2SO3,C项错误;D.溶液B加KSCN溶液呈血红色,说明含有Fe3+,加铁氰化钾显蓝色,证明含亚铁离子,所以该固体含有FeO和Fe2O3,D项正确;答案选D。

练习册系列答案
相关题目