题目内容
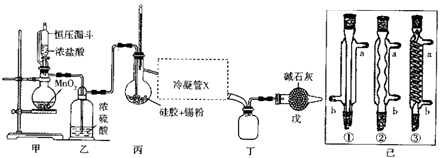
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO33H2O.实验过程如图1: 
(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)═Mg2+(aq)+CO2(g)+H2O(l)△H=﹣50.4kJmol﹣1
Mg2SiO4(s)+4H+(aq)═2Mg2+(aq)+H2SiO3(s)+H2O(l)△H=﹣225.4kJmol﹣1
酸溶需加热的目的是_;所加H2SO4不宜过量太多的原因是 .
(2)加入H2O2氧化时发生发应的离子方程式为
(3)用图2所示的实验装置进行萃取分液,以除去溶液中的Fe3+ .
①实验装置图中仪器A的名称为 .
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,、静置、分液,并重复多次.
(4)请补充完整由萃取后得到的水溶液制备MgCO33H2O的实验方案:边搅拌边向溶液中滴加氨水, , 过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO33H2O.
已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全].
【答案】
(1)加快反应(酸溶)速率;避免制备MgCO3时消耗更多的碱
(2)H2O2+2Fe2++2H+═2Fe3++2H2O
(3)分液漏斗;充分振荡
(4)至5<pH<8.5,过滤,边搅拌边向滤液中滴加碳酸钠溶液至有大量沉淀生成,静置,向上层清夜中滴加碳酸钠溶液,若无沉淀生成
【解析】解:废渣主要成分为MgCO3、MgSO4和少量Fe、Al的氧化物,加入40%的硫酸酸溶,过量后滤液中含有硫酸镁、硫酸亚铁、硫酸铝和过量的硫酸,加入H2O2氧化亚铁离子,然后加入有机萃取剂萃取Fe3+ , 分液后可除去溶液中的Fe3+ , 分液后水溶液中含有Mg2+、Al3+ , 可调节溶液pH至5<pH<8.5,可除去Al3+ , 又可防止生成Mg(OH)2 , 过滤后在滤液中加入碳酸钠溶液,可生成MgCO3沉淀,在50℃下干燥,得到MgCO33H2O.(1)酸溶需加热的目的是加快反应(酸溶)速率;H2SO4不宜过量太多的避免制备MgCO3时消耗更多的碱;所以答案是:加快反应(酸溶)速率;避免制备MgCO3时消耗更多的碱;(2)在酸性条件下,H2O2氧化亚铁离子为铁离子,本身被还原为水,反应的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
所以答案是:H2O2+2Fe2++2H+═2Fe3++2H2O;(3)①仪器A为分液漏斗;
所以答案是:分液漏斗;②萃取时,为使溶质尽可能被萃取,应充分振荡,以充分接触而分离;
所以答案是:充分振荡;(4)分液后水溶液中含有Mg2+、Al3+ , 可调节溶液pH至5<pH<8.5,可除去Al3+ , 又可防止生成Mg(OH)2 , 过滤后在滤液中加入碳酸钠溶液,可生成MgCO3沉淀,静置,向上层清夜中滴加碳酸钠溶液,若无沉淀生成,说明已完全反应,过滤后,用水洗涤固体2﹣3次,在50℃下干燥,得到MgCO33H2O;
所以答案是:至5<pH<8.5,过滤,边搅拌边向滤液中滴加碳酸钠溶液至有大量沉淀生成,静置,向上层清夜中滴加碳酸钠溶液,若无沉淀生成.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性.
实验 | 试剂 | 现象 | |
滴管 | 试管 | ||
| 0.2 molL﹣1 Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
0.2 molL﹣1 CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | ||
0.1 molL﹣1 Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | ||
(1)经检验,现象Ⅰ中的白色沉淀是Ag2SO3 . 用离子方程式解释现象Ⅰ: .
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO42﹣ , 含有Cu+、Cu2+和SO32﹣ .
已知:Cu+ ![]() Cu+Cu2+ , Cu2+
Cu+Cu2+ , Cu2+ ![]() CuI↓(白色)+I2 .
CuI↓(白色)+I2 .
①用稀硫酸证实沉淀中含有Cu+的实验现象是 .
②通过下列实验证实,沉淀中含有Cu2+和SO32﹣ . 
a.白色沉淀A是BaSO4 , 试剂1是 .
b.证实沉淀中含有Cu2+和SO32﹣的理由是 .
(3)已知:Al2(SO3)3在水溶液中不存在.经检验,现象Ⅲ的白色沉淀中无SO42﹣ , 该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色.
①推测沉淀中含有亚硫酸根和 .
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.被Al(OH)3所吸附;ii.存在于铝的碱式盐中.对假设ii设计了对比实验,证实了假设ii成立.
a.将对比实验方案补充完整.
步骤一: 
步骤二:(按图形式呈现).
b.假设ii成立的实验证据是
(4)根据实验,亚硫酸盐的性质有 . 盐溶液间反应的多样性与有关.
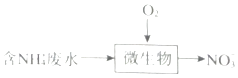
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3﹣)已成为环境修复研究的热点之一.
(1)Fe还原水体中NO3﹣的反应原理如图1所示. 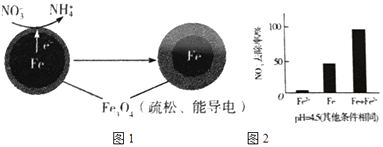
②作负极的物质是 .
②正极的电极反应式是 .
(2)将足量铁粉投入水体中,经24小时测定NO3﹣的去除率和pH,结果如表:
初始pH | pH=2.5 | pH=4.5 |
NO3﹣的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
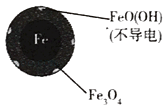
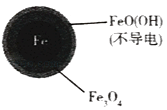
铁的最终物质形态 |
|
|
pH=4.5时,NO3﹣的去除率低.其原因是 .
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3﹣的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3﹣;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如右图2所示,可得到的结论是 .
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4 . 结合该反应的离子方程式,解释加入Fe2+提高NO3﹣去除率的原因: . pH=4.5(其他条件相同)