题目内容
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一,对下列实验现象或实验操作的解释正确的是
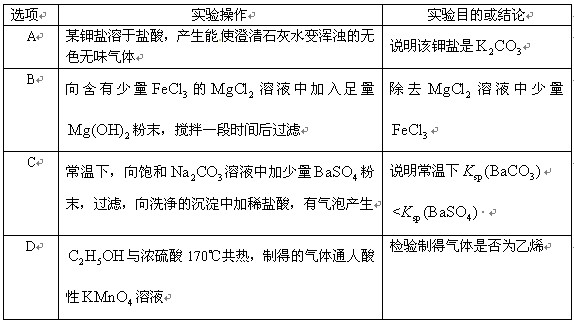
| | 现象或操作 | 解释 |
| A | 将氯化铁固体溶入加有盐酸的水中配制氯化铁溶液 | 抑制Fe3+的水解 |
| B | 某溶液中加入稀盐酸,放出无色无味气体,将气体通入澄清石灰水,石灰水变浑浊 | 该溶液中存在CO32- |
| C | 溴水中加入甲苯,充分振荡后静置,溴水层褪色 | 甲苯与溴水发生了取代反应 |
| D | 铝箔在酒精灯火焰上加热熔化但不滴落 | 氧化铝熔点高,兜住熔融的铝 |
AD
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


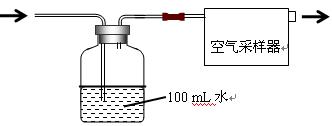
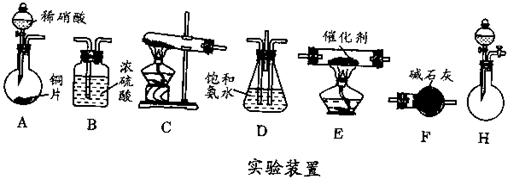
 口或橡皮管均已略去)完成该实验,若气体流向为从左到右,则正确的连接顺序是:
口或橡皮管均已略去)完成该实验,若气体流向为从左到右,则正确的连接顺序是:
 ____________________。
____________________。 验,反应结束后,测其实验前后的质量,由此得到乙烯产量。
验,反应结束后,测其实验前后的质量,由此得到乙烯产量。 方案II:将E及其后面的装置拆除后,连接图28—2所示装置进行实验,反应结束后,测得乙烯的体积,由此算得乙烯产量。
方案II:将E及其后面的装置拆除后,连接图28—2所示装置进行实验,反应结束后,测得乙烯的体积,由此算得乙烯产量。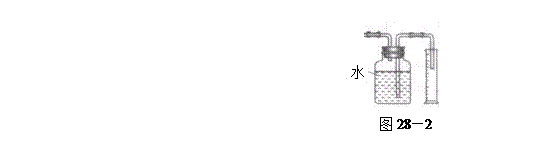
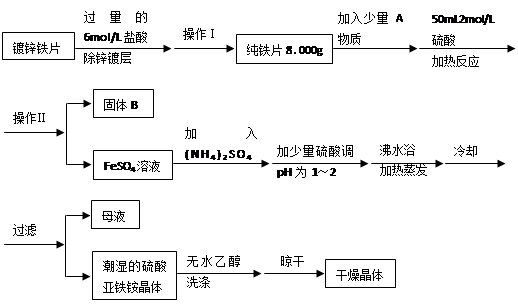
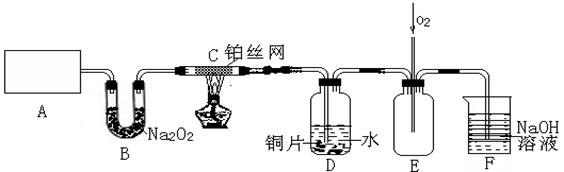 (3)D中铜片发生反应的离子方程式为___________________________,为了使Cu片溶解的速率加快,可向D处的溶液中加入下列少量物质中的___________(填下列各项序号)
(3)D中铜片发生反应的离子方程式为___________________________,为了使Cu片溶解的速率加快,可向D处的溶液中加入下列少量物质中的___________(填下列各项序号) _____________。
_____________。
 (OH)2(过量) 10.8g(NH4)2SO4
(OH)2(过量) 10.8g(NH4)2SO4
 ____________。
____________。