题目内容
下列说法中,正确的是
| A.第ⅠA族元素都比第ⅡA族元素金属性强 |
| B.只含有非金属元素的化合物可能是离子化合物 |
| C.只含有共价键的物质一定是共价化合物 |
| D.同主族元素原子半径越小越容易失去电子 |
B
解析试题分析:A、在同一周期中,第ⅠA族元素都比第ⅡA族元素金属性强,错误;B、如氯化铵化合物中只有非金属元素,形成的是离子化合物,正确;C、只含有共价键的物质有可能是单质,不一定是化合物,错误;D、同主族元素原子半径越大越容易失去电子,错误。
考点:考查金属性及非金属性强弱变化的规律,化合物中化学键的类型。

练习册系列答案
相关题目
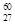 Co是r射线的放射源,关于
Co是r射线的放射源,关于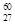 27Co的说法正确的是
27Co的说法正确的是
| A.质子数为 33 | B.中子数为27 | C.质量数为60 | D.核电荷数为60 |
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是
| A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.X的最高价氧化物对应水化物的酸性比W的弱 |
| D.Y的气态简单氢化物的热稳定性比W的强 |
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是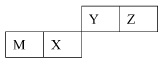
| | Y | Z | |
| M | X | | |
B.Y的最高价氧化物对应水化物的酸性比X 的弱
C.X 的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2 周期、第ⅥA族
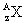 与
与 的两种微粒,下列叙述正确的是( )
的两种微粒,下列叙述正确的是( )
| A.一定都是由质子、中子、电子组成的 |
| B.化学性质几乎完全相同 |
| C.核电荷数和核外电子数一定相等 |
| D.质子数一定相同,质量数和中子数一定不相同 |
香花石被誉为“矿石熊猫”,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是:( )
| A.原子半径:Y>Z>R>T |
| B.气态氢化物的稳定性:W<R<T |
| C.最高价氧化物对应的水化物碱性:X>Z |
| D.XR2、WR2两化合物中R的化合价相同 |
下列顺序正确的是( )
| A.熔点:SiO2< NaF<KCl | B.水溶性:NH3<SO2<HCl |
| C.酸性:HF>HCl>HI | D.碱性:Mg(OH)2<KOH<RbOH |
X、Y、Z是短周期的三种主族元素,在周期表中的相对位置如图所示,下列说法正确的是
| X | |
| Y | Z |
A.原子半径:X<Y<Z
B.X、Y、Z三种元素的最高价氧化物对应水化物中最多有一种强酸
C.X的气态氢化物的稳定性比Y的气态氢化物强
D.常温下X、Y、Z的单质不可能均与盐酸反应