题目内容
【题目】2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99 kJ·![]() 。请回答下列问题:
。请回答下列问题:
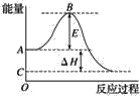
(1)图中A、C分别表示__,E的大小对该反应的反应热__(填“有”或“无”)影响.该反应通常用V2O5作催化剂,加V2O5会使图中B点__(填“升高”或“降低”),ΔH__(填“变大”“变小”或“不变”)。
(2)图中ΔH=__kJ·![]() 。
。
【答案】反应物总能量;生成物总能量 无 降低 不变 -198
【解析】
(1)反应物总能量大于生成物总能量,为放热反应,加入催化剂,活化能减小,反应热不变;
(2)根据反应2SO2(g)+O2(g)=2SO3(g)结合1mol SO2(g)氧化为1mol SO3的△H=-99kJmol-1计算反应热。
(1)图中A、C分别表示反应物总能量、生成物总能量。B为活化能,反应热可表示为A、C活化能的大小之差,活化能的大小与反应热无关。加入催化剂能降低反应的活化能,加快化学反应速率,但不改变ΔH。
(2)因1 mol SO2(g)氧化为1 mol SO3的ΔH=-99 kJ·![]() ,所以2 mol SO2(g)氧化为2 mol SO3的ΔH=-198 kJ·
,所以2 mol SO2(g)氧化为2 mol SO3的ΔH=-198 kJ·![]() ,则2SO2(g)+O2(g)=2SO3(g)ΔH=-198 kJ·
,则2SO2(g)+O2(g)=2SO3(g)ΔH=-198 kJ·![]() 。
。

练习册系列答案
相关题目