��Ŀ����
9������һ��������Na2O���ʵ�Na2O2����������ͼ��ʵ��װ�òⶨNa2O2�����Ĵ��ȣ����ɹ�ѡ�õķ�Ӧ��ֻ��CaCO3���塢6mol/L���ᡢ6mol/L���������ˮ��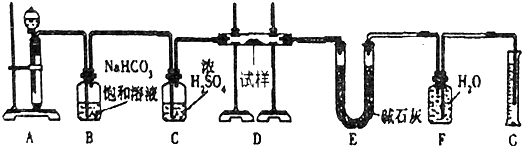
�ش��������⣺
��1��ʵ��ǰ��������װ�õ������ԣ�
��2��װ��A��Һ���Լ�ѡ��������������ᣬ�����������̼��Ʒ�Ӧ���ɵ������������ˮ�ģ��Ḳ����̼��Ƶı��棬ʹ��Ӧ���ܳ�����
��3��װ��B�������dz�ȥ�����е�HCl��
װ��C�������Ǹ������壻
װ��E�м�ʯ�ҵ�����������װ��D�з�Ӧʣ��Ķ�����̼��
��4��װ��D�з�����Ӧ�Ļ�ѧ����ʽ�ǣ�Na2O+CO2=Na2CO3��2Na2O2+2CO2=2Na2CO3+O2��
��5������ʼʱ�����Ʒ������Ϊ2.0g����Ӧ���������������Ϊ224mL����״��������Na2O2�����Ĵ���Ϊ78%��
���� ��1����װ�������������еIJ���Ϊ���װ�õ������ԣ�
��2������ʵ��ԭ��װ��A���õ���̼��ƺ����ᷴӦ���ɶ�����̼������̼��ƺ����ᷴӦ��������ش�
��3����õĶ�����̼�����к����Ȼ������壬�����ñ���̼����������ȥ��Ũ���������ˮ�ԣ���ʯ�ҿ������ն�����̼��
��4��װ��D���ǹ������ƺͶ�����̼������̼���ƺ������������ƺͶ�����̼��Ӧ����̼���ƣ�
��5�������������������������Ĺ�ϵ����ù���������������������������ƵĴ��ȣ�
��� �⣺��1����װ�������������еIJ���Ϊ���װ�õ������ԣ��ʴ�Ϊ�����װ�õ������ԣ�
��2��װ��A��̼��ƺ����ᷴӦ���ɶ�����̼��̼��ƺ����ᷴӦʱ�����ɵ������������ˮ�ģ��Ḳ����̼��Ƶı��棬ʹ��Ӧ���ܳ����������������������������Ӧ���ʴ�Ϊ�������̼��Ʒ�Ӧ���ɵ������������ˮ�ģ��Ḳ����̼��Ƶı��棬ʹ��Ӧ���ܳ�����
��3��̼��ƺ����ᷴӦ���ɵĶ�����̼�����к����Ȼ������壬�����ñ���̼����������ȥ��Ũ���������ˮ�ԣ����Խ�������̼���װ��E�м�ʯ�ҵ����������ն�����̼����ֹ�����������������ɸ��ţ�
�ʴ�Ϊ����ȥ�����е�HCl���������壻����װ��D�з�Ӧʣ��Ķ�����̼��
��4��װ��D���ǹ������ƺͶ�����̼������̼���ƺ������������ƺͶ�����̼��Ӧ����̼���ƣ���Ӧ�Ļ�ѧ����ʽΪ��Na2O+CO2=Na2CO3��
2Na2O2+2CO2=2Na2CO3+O2��
�ʴ�Ϊ��Na2O+CO2=Na2CO3��2Na2O2+2CO2=2Na2CO3+O2��
��5�����ݷ�Ӧ2Na2O2+2CO2=2Na2CO3+O2����Ӧ���������������Ϊ224mL����״�����������ɵ���������0.01mol���������Ƶ����ʵ���Ϊ0.02mol��
�������ƵĴ���=$\frac{0.02mol��78g/mol}{2.0g}$��100%=78%���ʴ�Ϊ��78%��
���� ���⿼��ѧ���������ƵĻ�ѧ����֪ʶ��ͨ��ʵ�鷽ʽ�����������Ѷȣ��ۺ��Խ�ǿ����Ŀ�Ѷ��еȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | ������Ϊ17��������Ϊ20����ԭ�ӣ�${\;}_{17}^{20}$Cl | |
| B�� | �����ӣ�Cl-���Ľṹʾ��ͼ��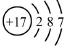 | |
| C�� | �ȷ��ӵĵ���ʽ��${\;}_{•}^{•}$$\underset{\stackrel{••}{Cl}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{Cl}}{••}$${\;}_{•}^{•}$ | |
| D�� | ����ϩ���ӵĽṹ��ʽ��H3C-CH2Cl |
| X�Ļ�̬ԭ���е��ӷֲ���������ͬ���ܼ��У���ÿ���ܼ��еĵ���������ͬ |
| YԪ�ص����������������������� |
| ZԪ�صĵ縺��������Ԫ������� |
| Wԭ�ӵĵ�һ�����������ֱܷ�Ϊ��I1=578KJ•mol-1��I2=1817KJ•mol-1��I3=2745KJ•mol-1��I4=11575KJ•mol-1��I5=14830KJ•mol-1��I6=18376KJ•mol-1 |
| QΪǰ�������е縺����С��Ԫ�� |
| Rԭ������ܲ���ֻ��1�������ӣ�������ܲ���ѳ������ӣ� |
��1��R�����ڱ���λ��ds����д��R��̬ԭ�ӵļ۵����Ų�ʽ3d104s1��
��2��X��Y�γɵĶ�Ԫ�����������ڷǼ��Է��ӵ�CO2 ���û�ѧʽ��ʾ����
��3��д��ZԪ�صĵ�����ˮ��Ӧ�ķ�ʽ2F2+2H2O=4HF+O2���˷�Ӧ���������������������ʵ���֮��Ϊ2��1��
��4��X���Ȼ�����۵��Q���Ȼ�����۵�ͣ����ߡ��͡�����������CCl4���ڷ��Ӿ��壬KCl�������Ӿ��壮
��5������֤ʵ����W��ǿ������Һ��Ӧ��[W��OH��4]-���ɣ�����[W��OH��4]--����acd����ѡ����ĸ��
a�����Թ��ۼ� b���Ǽ��Թ��ۼ� c����λ�� d���Ҽ� e���м�
��6�����ɰ��SiC���Ľṹ����ʯ��4��̼ԭ�������������ڣ�����̼ԭ�ӷֱ�λ�����ĺͶ��ǣ����ƣ�Ӳ������ʯ�൱������ɰ�ľ����к���4����ԭ�ӣ�4��̼ԭ�ӣ����й�ԭ�ӵ��ӻ���ʽΪsp3��
| A�� | ԭ���ƴ���̼���� | |
| B�� | ���ƴ�������ܴ�Ӧ�� | |
| C�� | ���ƴ��ij���������� | |
| D�� | ���ƴ������������棬���������������ɿ������Ȼ��� |
| A�� | ��������ƽ����11.7g�Ȼ��ƾ��� | |
| B�� | �ü�ʽ�ζ�����ȡ25.00mL���������Һ | |
| C�� | �����ô����������������ơ�̼���� | |
| D�� | �ⶨ��Һ��pHʱ���ýྻ������IJ�����պȡ��Һ������������ˮ��ʪ����pH��ֽ�ϣ��������ɫ���Ƚ� | |
| E�� | ������ˮ��pH��ֽ���Ϳ��Լ���pH��ȵ�H2SO4��CH2COOH��Һ |
| A�� |  | B�� | Na+ | C�� | 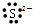 | D�� | 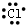 |
ijͬѧ��ȡ10.00g��Ʒ�����1000mL��Һ���ü�ʽ�ζ��ܣ����������ƣ���ȡ25.00mL������ƿ�У����������ָʾ������0.1500mol•L-1������ζ����յ㣮ƽ�вⶨ���Σ��й�ʵ�����ݼ�¼���������Ʒ��̼���Ƶ���������Ϊ95.4%��
| ������ | ����Һ�����mL�� | ��Һ�����mL�� | |
| �ζ�ǰ���� | �յ�ʱ���� | ||
| 1 | 25.00 | 0.00 | 30.02 |
| 2 | 25.00 | 0.20 | 33.80 |
| 3 | 25.00 | 1.40 | 31.38 |
| һ������ | ����ԭ�ӵ����༰����Ŀ | ԭ������ | �������� |
| O2 | |||
| H2O | |||
| NH3 | |||
| H2SO4 |
| A�� | H2SO4��Ħ��������98 | |
| B�� | 0.5mol H2SO4�к�6.02��1023��H | |
| C�� | 1mol H2SO4�к�2mol O2 | |
| D�� | 3.01��1023��H2SO4���ӵ�����Ϊ49g/mol |