题目内容
在进行胃部透视时,为取得良好的检查效果,需要在检查之前服用“钡餐”,“钡餐”的主要成分是硫酸钡.在25℃时,1L水中约能溶解2.4×10-3g 硫酸钡,它的溶度积常数Ksp=1.1×10-10.(1)钡离子是一种有毒的重金属离子,当人体中钡离子浓度达到2×10-3mol?L-1时,就会对健康产生危害.请通过计算说明为什么可以用硫酸钡作为“钡餐”.
(2)在25℃时,1L水中约能溶解0.018g 碳酸钡,且胃液是酸性的,能否用碳酸钡代替硫酸钡作为“钡餐”的主要成分?
【答案】分析:(1)根据硫酸钡的溶度积常数计算硫酸钡溶液中的钡离子浓度,判断是否对人体有害;
(2)根据碳酸钡能溶解于胃酸分析能否代替.
解答:解:(1)根据硫酸钡的溶解平衡计算,在硫酸钡中存在平衡:BaSO4(s)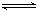 Ba2+(aq)+SO42-(aq),
Ba2+(aq)+SO42-(aq),
c(Ba2+)= =1.05×10-5mol?L-1,小于2×10-3 mol?L-1,而胃液中H+对BaSO4的沉淀溶解平衡没有影响,所以BaSO4可用做“钡餐”,
=1.05×10-5mol?L-1,小于2×10-3 mol?L-1,而胃液中H+对BaSO4的沉淀溶解平衡没有影响,所以BaSO4可用做“钡餐”,
答:由BaSO4(s) Ba2+(aq)+SO42-(aq),c(Ba2+)=1.05×10-5mol?L-1<2×10-3 mol?L-1,胃液中H+对BaSO4的沉淀溶解平衡没有影响,因此BaSO4可用做“钡餐”;
Ba2+(aq)+SO42-(aq),c(Ba2+)=1.05×10-5mol?L-1<2×10-3 mol?L-1,胃液中H+对BaSO4的沉淀溶解平衡没有影响,因此BaSO4可用做“钡餐”;
(2)胃酸的主要成分是盐酸,盐酸能与CO32-反应生成二氧化碳和水,促进BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大而引起人体中毒,
答:因BaCO3(s) Ba2+(aq)+CO32-(aq),由于胃液是酸性的,如果服下BaCO3,胃酸可与CO32-反应生成二氧化碳和水,使CO32-的浓度降低,从而使BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大而引起人体中毒.
Ba2+(aq)+CO32-(aq),由于胃液是酸性的,如果服下BaCO3,胃酸可与CO32-反应生成二氧化碳和水,使CO32-的浓度降低,从而使BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大而引起人体中毒.
点评:本题考查难溶电解质的溶解平衡,题目难度不大,本题中注意碳酸比盐酸弱,盐酸与碳酸钡反应的问题.
(2)根据碳酸钡能溶解于胃酸分析能否代替.
解答:解:(1)根据硫酸钡的溶解平衡计算,在硫酸钡中存在平衡:BaSO4(s)
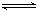 Ba2+(aq)+SO42-(aq),
Ba2+(aq)+SO42-(aq),c(Ba2+)=
 =1.05×10-5mol?L-1,小于2×10-3 mol?L-1,而胃液中H+对BaSO4的沉淀溶解平衡没有影响,所以BaSO4可用做“钡餐”,
=1.05×10-5mol?L-1,小于2×10-3 mol?L-1,而胃液中H+对BaSO4的沉淀溶解平衡没有影响,所以BaSO4可用做“钡餐”,答:由BaSO4(s)
 Ba2+(aq)+SO42-(aq),c(Ba2+)=1.05×10-5mol?L-1<2×10-3 mol?L-1,胃液中H+对BaSO4的沉淀溶解平衡没有影响,因此BaSO4可用做“钡餐”;
Ba2+(aq)+SO42-(aq),c(Ba2+)=1.05×10-5mol?L-1<2×10-3 mol?L-1,胃液中H+对BaSO4的沉淀溶解平衡没有影响,因此BaSO4可用做“钡餐”;(2)胃酸的主要成分是盐酸,盐酸能与CO32-反应生成二氧化碳和水,促进BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大而引起人体中毒,
答:因BaCO3(s)
 Ba2+(aq)+CO32-(aq),由于胃液是酸性的,如果服下BaCO3,胃酸可与CO32-反应生成二氧化碳和水,使CO32-的浓度降低,从而使BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大而引起人体中毒.
Ba2+(aq)+CO32-(aq),由于胃液是酸性的,如果服下BaCO3,胃酸可与CO32-反应生成二氧化碳和水,使CO32-的浓度降低,从而使BaCO3的沉淀溶解平衡向右移动,使Ba2+浓度增大而引起人体中毒.点评:本题考查难溶电解质的溶解平衡,题目难度不大,本题中注意碳酸比盐酸弱,盐酸与碳酸钡反应的问题.

练习册系列答案
相关题目
 Ba2+(aq)+SO42-(aq)
Ba2+(aq)+SO42-(aq)