题目内容
2.①升高温度 ②增大反应物浓度 ③将块状固体反应物磨成粉末 ④减小压强,上述影响化学反应速率的外界因素中,肯定能使化学反应速率加快的是( )| A. | ①②③④ | B. | 仅①②③ | C. | 仅①③④ | D. | 仅①②④ |
分析 一般来说,增大浓度、升高温度、增大压强、加入催化剂或增大固体的表面加等都可增大反应速率,以此解答该题.
解答 解:①升高温度,活化分子百分数增加,则反应速率增大,故正确;
②增大反应物浓度,单位体积的活化分子的数目增多,则反应速率增大,故正确;
③将块状固体反应物磨成粉末,固体表面积增大,反应速率增大,故正确;
④减小压强,如没有气体参加反应,则反应速率不变,如有气体参加反应,则反应速率减小,故错误.
故选B.
点评 本题考查化学反应速率的影响,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,易错点为④,注意压强只影响有气体参加的反应,难度不大.

练习册系列答案
相关题目
10.A和M为两种元素,已知A位于短周期,且A2+与M-的电子数之差为8,则下列说法正确的是( )
| A. | A和M的原子序数之差为6 | |
| B. | A和M原子的最外层电子数之差为7 | |
| C. | A和M原子的最外层电子数之和可能为9 | |
| D. | A和M原子的电子总数之和可能为11 |
17.用化学用语表达下列微粒,错误的是( )
| A. | 氟离子的结构示意图: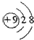 | |
| B. | 氮分子的电子式: | |
| C. | 水分子的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| D. | C-14原子:${\;}_{6}^{14}$C |
7.下列离子方程式正确的是( )
| A. | 稀硝酸与氢氧化钾溶液反应 H++OH-→H2O | |
| B. | 铝与稀盐酸反应 Al+2H+→Al3++H2↑ | |
| C. | 氯化铁溶液与氢氧化钠溶液反应 FeCl3+3OH-→Fe(OH)3↓+3C1- | |
| D. | 二氧化碳与石灰水反应 CO2+2OH-→CO32-+H2O |
14.在2L密闭容器中,盛有2mol X和2molY物质进行如下反应:X(s)+3Y(g)?Z(g),当反应进行到10s后,测得生成0.5mol Z,这期间的平均反应速率为( )
| A. | v(X)=0.5mol•s-1 | B. | v(X)=0.025mol•L-1•s-1 | ||
| C. | v(y)=0.05mol•L-1•s-1 | D. | v(y)=0.075mol•L-1•s-1 |
11.将纯锌片和纯铜片按如图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )

| A. | 甲烧杯中锌片逐渐溶解,乙烧杯中锌片不溶解 | |
| B. | 两烧杯中铜片表面均无气泡产生 | |
| C. | 两烧杯中溶液的酸性均减弱 | |
| D. | 甲烧杯中铜片上的电极反应为:Cu2++2e-=Cu |
12.下列气体的主要成分不是甲烷的是( )
| A. | 坑道气 | B. | 煤气 | C. | 天然气 | D. | 沼气 |

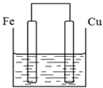 将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图的装置(以下均假设反应过程中溶液体积不变).
将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图的装置(以下均假设反应过程中溶液体积不变).