题目内容
20.氢化铵(NH4H)与氯化铵的结构相似,它与水反应有气体生成.下列关于氢化铵叙述不正确的是( )| A. | 是离子化合物,含有离子键和共价键 | |
| B. | 电子式是 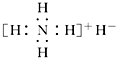 | |
| C. | 与水反应时,它既是还原剂又是氧化剂 | |
| D. | 固体投入少量的水中,有两种气体产生 |
分析 A.依据氯化铵,可知氢化铵是由氨根离子与氢负离子构成;
B.NH4H是离子化合物,由铵根离子与氢负离子构成;
C.NH4H与水发生了氧化还原反应,氢负离子化合价升高,被氧化,NH4H做还原剂;
D.NH4H固体投入少量水中,可生成NH3和H2.
解答 解:A.氢化铵中铵根离子与氢负离子之间存在离子键,氨根离子内部存在N-H共价键,故A正确;
B.NH4H是离子化合物,由铵根离子与氢负离子构成,电子式为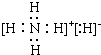 ,故B错误;
,故B错误;
C.NH4H中含有-1价H,与水反应时发生氧化还原生成氢气,NH4H为还原剂,发生氧化反应,故C错误;
D.NH4H固体投入少量水中,与水反应生成成NH3和H2,故D正确;
故选:BC.
点评 本题考查了铵盐的性质与结构,明确氢化铵的结构及性质是解题关键,注意氢化铵中所含氢元素化合价,题难度不大.

练习册系列答案
相关题目
10.下列物质露置在空气中,质量会减轻的是( )
| A. | NaOH | B. | 浓H2SO4 | C. | Na2O2 | D. | 浓盐酸 |
8.下列反应的有机产物中只有一种的是( )
| A. | CH3CH═CH2与HCl加成 | B. | CH3CH2CH2Cl在碱性溶液中水解 | ||
| C. | CH3CH2OH与浓H2SO4混合加热 | D. | CH3CHBrCH2CH3与NaOH醇溶液共热 |
15.下列说法中正确的是( )
| A. | KOH中含有离子键也含有共价键,属于离子化合物 | |
| B. | HCl中存在离子键,属于离子化合物 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 阴、阳离子间通过静电引力而形成的化学键叫做离子键 |
5.下列化学用语正确的是( )
| A. | 氯化氢的电子式: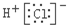 | B. | N2的结构式:N≡N | ||
| C. | 硫离子结构示意图: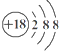 | D. | 四氯化碳的电子式: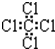 |
19.某阴离子X2-有m个电子,其质量数为a,则核内中子数为( )
| A. | m+2 | B. | m+5 | C. | a-m+2 | D. | a-m-2 |


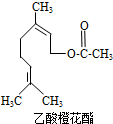 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中不正确的是( )