题目内容
【题目】向50ml物质的量浓度均为0.1mol/L (NH4)2SO4、Al2(SO4)3溶液中逐滴滴入0.1mol/L Ba(OH)2溶液200ml,随着Ba(OH)2溶液体积的变化,沉淀总物质的量(n)的变化如图所示。下列叙述不正确的是
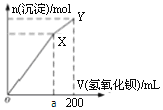
A.a=150
B.Y点对应溶液为氨水
C.OX、XY两段沉淀种类相同
D.继续滴加Ba(OH)2溶液,发生的离子反应为Al(OH)3+OH-=AlO2-+2H2O
【答案】C
【解析】
试题分析:50mL0.1molL-1(NH4)2SO4、Al2(SO4)3溶液,溶液含有NH4+0.01mol,Al3+0.01mol,SO42-0.02mol。开始滴加同时发生反应为SO42-+Ba2+=BaSO4↓,Al3++3OH-=Al(OH)3↓,当Al3+沉淀完全时需加入0.03molOH-,即加入0.015molBa(OH)2,加入的Ba2+为0.015mol,SO42-未完全沉淀,此时溶液含有硫酸铵;再滴加Ba(OH)2,生成BaSO4沉淀,发生反应为SO42-+Ba2+=BaSO4↓,NH4++OH-=NH3H2O,所以沉淀质量继续增加,但增加幅度较前一过程小;当SO42-完全沉淀时,共需加入0.02molBa(OH)2,加入0.04molOH-,Al3+反应掉0.03molOH-,生成Al(OH)30.01mol,剩余0.01molOH-恰好与NH4+完全反应,此时溶液中NH4+完全反应,此时溶液为氨水溶液,沉淀达最大为BaSO4和Al(OH)3;继续滴加Ba(OH)2,Al(OH)3溶解。A.根据上述分析,a点对应0.015molBa(OH)2,氢氧化钡的体积为![]() =0.15L=150mL,故A正确;B.根据上述分析,Y点对应溶液为氨水,故B正确;C.OX段的沉淀为硫酸钡和氢氧化铝、XY段的沉淀为硫酸钡,两段沉淀种类不相同,故C错误;D.根据上述分析,继续滴加Ba(OH)2溶液,Al(OH)3溶解,发生的离子反应为Al(OH)3+OH-=AlO2-+2H2O,故D正确;故选C。
=0.15L=150mL,故A正确;B.根据上述分析,Y点对应溶液为氨水,故B正确;C.OX段的沉淀为硫酸钡和氢氧化铝、XY段的沉淀为硫酸钡,两段沉淀种类不相同,故C错误;D.根据上述分析,继续滴加Ba(OH)2溶液,Al(OH)3溶解,发生的离子反应为Al(OH)3+OH-=AlO2-+2H2O,故D正确;故选C。

 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
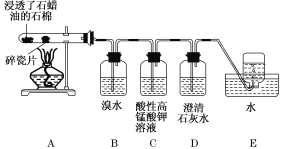
同步奥数系列答案【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。

发生的反应如下:
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0g Na2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,并说明理由 。
(2)加入沸石的作用是 。若加热后发现未加沸石,应采取的正确方法 是 。
(3)上述装置图中,B的名称是 ,D仪器的名称是 。
(4)B仪器使用前必须进行的操作是 。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分液时,正丁醛在 层(填“上”或“下”)
(6)反应温度应保持在90—95℃,其原因是 ,为更好的控制温度,可以采取的改进措施是 。
(7)本实验中,正丁醛的产率为 %。