��Ŀ����
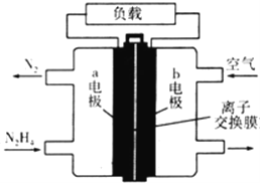
����Ŀ��Ԫ��A��B��C���Ƕ�����Ԫ�أ�AԪ��ԭ�ӵ�2p�����ֻ������δ�ɶԵ��ӣ�B��3p������пչ����A��Bͬ���壬B��Cͬ���ڣ�C�DZ������е縺�����ģ�
��ش�
��1��Aԭ�ӵĺ�������Ų��ĵ����Ų�ͼ ______________ ��Bԭ�ӵĺ�������Ų�ʽ________��Cԭ�ӵļ۵����Ų�ʽ____________��
��2��A��B��C����̬�⻯��Ļ�ѧʽ�ֱ���___________��������ȶ�����__________��
��3�����ǵ�����������ˮ�����У�������ǿ����_________��
��4��AC4�Ļ�ѧʽ___________���ṹʽ__________������ԭ��A���ӻ���ʽ________�ӻ�����__________�����������������Ǽ�������������
���𰸡�![]() 1s22s22p63s23p2 3s23p5 CH4��SiH4��HCl SiH4 HClO4 CCl4��
1s22s22p63s23p2 3s23p5 CH4��SiH4��HCl SiH4 HClO4 CCl4��  sp3 �Ǽ���
sp3 �Ǽ���
��������
Ԫ��A��B��C���Ƕ�����Ԫ�أ�AԪ��ԭ�ӵ�2p�����ֻ������δ�ɶԵ��ӣ���A����Χ�����Ų�Ϊ2s22p2����AΪ̼Ԫ�أ�B��3p������пչ������B��A����Χ�����Ų�Ϊ3s23p1��3s23p2��A��Bͬ���壬��BΪ��Ԫ�أ�B��Cͬ���ڣ�C�DZ������е縺�����ģ���CΪ��Ԫ�ء�
��1��AΪ̼Ԫ�أ�Cԭ�ӵĺ�������Ų��Ĺ����ʾʽ![]() ��Bԭ��ΪSiԪ�أ�Si�ĺ�������Ų�ʽΪ��1s22s22p63s23p2��CΪClԪ�أ�Clԭ�ӵļ۵����Ų�ʽΪ��3s23p5���ʴ�Ϊ��
��Bԭ��ΪSiԪ�أ�Si�ĺ�������Ų�ʽΪ��1s22s22p63s23p2��CΪClԪ�أ�Clԭ�ӵļ۵����Ų�ʽΪ��3s23p5���ʴ�Ϊ��![]() ��1s22s22p63s23p2��3s23p5��
��1s22s22p63s23p2��3s23p5��
��2��A��B��C�γɵ���̬�⻯��ֱ�Ϊ��CH4��SiH4��HCl����Ϊ�ǽ�����Cl��C��Si�����ڷǽ�����Խǿ������̬�⻯��Խ�ȶ�������Щ�⻯������ȶ�����SiH4���ʴ�Ϊ��SiH4��
��3��A��B��C�γɵ�����������ˮ�������ۺ����ᣩ�ֱ�Ϊ��H2CO3��H2SiO3��HClO4�����ڷǽ�����Խǿ��������Խǿ����������ǿ���ǣ�HClO4���ʴ�Ϊ��HClO4��
��4��AC4ΪCCl4����ṹʽ��������飬Ϊ�������壬��Ϊ ����������Cԭ�Ӳ�ȡsp3�ӻ���CCl4�������ɼ��Լ����ɵķǼ��Է��ӣ��ʴ�Ϊ��
����������Cԭ�Ӳ�ȡsp3�ӻ���CCl4�������ɼ��Լ����ɵķǼ��Է��ӣ��ʴ�Ϊ�� ��sp3���Ǽ��ԡ�
��sp3���Ǽ��ԡ�

 ��ѧ��������������Ͼ���ѧ������ϵ�д�
��ѧ��������������Ͼ���ѧ������ϵ�д� �ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
�ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�����Ŀ�������ֶ�����Ԫ�أ����ǵĽṹ�����ʵ���Ϣ���±�������
Ԫ�� | �ṹ�����ʵ���Ϣ |
A | �Ƕ������У���ϡ�������⣩ԭ�Ӱ뾶����Ԫ�أ���Ԫ�ص�ij�ֺϽ���ԭ�ӷ�Ӧ�ѵĵ��ȼ� |
B | B��Aͬ���ڣ�������������ˮ��������� |
C | Ԫ�ص���̬�⻯�K������ˮ������������� |
D | �Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���Ҳ������ˮ���������г��õ�����ɱ���� |
����ݱ�����Ϣ��д��
��1��Aԭ�ӵĺ�������Ų�ʽ______��
��2�����Ӱ뾶��B____A����������������С��������
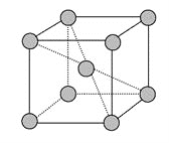
��3��Cԭ�ӵĵ����Ų�ͼ��____����ԭ�Ӻ�����___��δ�ɶԵ�����������ߵĵ���Ϊ___����ϵĵ��ӣ�������____����
��4��Dԭ�ӵ�����ռԭ�ӹ����Ϊ_______����D���Ľṹʾ��ͼ��_____��
��5��BD3��ˮ��Һ��______�ԣ�ԭ��_____________________�������ӷ���ʽ��ʾ����