��Ŀ����
����Ŀ��ʵ�������ܶ�Ϊ1.25 g mL-1����������Ϊ36.5%��Ũ��������240 mL 0.1 mol L-1�����ᣬ��ش��������⣺
��1��Ũ��������ʵ���Ũ��Ϊ ��
��2������ 240 mL 0.1 mol L-1������
Ӧ��ȡŨ�������/mL | Ӧѡ������ƿ�Ĺ��/mL |
��1������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ� ��
A����30 mLˮϴ���ձ��ڱںͲ�����23�Σ�ϴ��Һ��ע������ƿ����
B������Ͳ��ȷ��ȡ�����Ũ���������������ձ��У��ټ�������ˮ��Լ30 mL��, �ò���������������ʹ���Ͼ���
C��������ȴ�������ز�����ע������ƿ��
D��������ƿ�ǽ�����ҡ��
E.���ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶�������
F.����������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���12 cm��
��4����ʵ�������������������������Һ�����ʵ���Ũ���к�Ӱ�죨����ƫ��������ƫ������������������
������ϡ��������ձ�δϴ�ӣ� ��
������ƿ��ԭ����������ˮ�� ��
������ʱ�۲�Һ�温�ӣ� ��
��5����ʵ������г������������δ�����
������ʱ������ˮʱ�����˿̶� ��
��������ƿ��ת����Һʱ�й�Һ��������Һ���� ��
������ҡ�����Һ���½� ��
���𰸡���1��12.5mol/L����2��2.0��250����3��BCAFED��
��4����ƫ�ͣ������䣬��ƫ�ߣ�
��5�����������ƣ����������ƣ����������䡣
�������������������1��ʵ�������ܶ�Ϊ1.25 g mL-1����������Ϊ36.5%��Ũ��������240 mL 0.1 mol L-1�����ᣬ����ʵ����û��240mL������ƿ�������Ҫ����250mL��Һ��������HCl�����ʵ���Ϊ��n��HCl��=0.25L��0.1 mol L-1=0.025mol������HCl������Ϊ��m��HCl��=0.025mol��36.5g mol-1=0.9125g����Һ������Ϊ��![]() ������Һ�����
������Һ�����![]() ��������ʵ����ʵ���Ũ��Ϊ��
��������ʵ����ʵ���Ũ��Ϊ��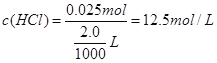 ����2��������������֪��Ӧ��ȡŨ��������Ϊ2.0mL����Ҫѡ������ƿ�Ĺ����250mL����ƿ����3��������Һʱ����һ��������Ͳ��ȷ��ȡ�����Ũ���������������ձ��У��ټ�������ˮ��Լ30 mL��, �ò���������������ʹ���Ͼ��ȣ��ڶ�����������ȴ�������ز�����ע������ƿ�У�����������30 mLˮϴ���ձ��ڱںͲ�����23�Σ�ϴ��Һ��ע������ƿ�������IJ�������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���12 cm�������岽�����ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶������У���������.������ƿ�ǽ�����ҡ�ȣ����װƿ���档��������Һ����ȷ˳����BCAFED ����4�����ݹ�ʽ��c=n/V������������������ϡ��������ձ�δϴ�ӣ�ʹ���ʵ����ʵ���ƫС����Һ������䣬�����Һ�����ʵ���Ũ��ƫ�ͣ�������ƿ��ԭ����������ˮ������Һ�����ƹ�����Ӱ�죬�����ʵ����ʵ���Ũ�Ȳ��䣻������ʱ�۲�Һ�温�ӣ���Һ�����ƫС��������ʵ����ʵ���Ũ��ƫ�ߡ���5��������ʱ������ˮʱ�����˿̶ȣ���������������Һ����������ƿ��ת����Һʱ�й�Һ��������Һ���������ʵ����ʵ���ƫС������������Һ�����ʵ���Ũ�Ȳ��������������ƣ�������ҡ�����Һ���½��������������ơ�
����2��������������֪��Ӧ��ȡŨ��������Ϊ2.0mL����Ҫѡ������ƿ�Ĺ����250mL����ƿ����3��������Һʱ����һ��������Ͳ��ȷ��ȡ�����Ũ���������������ձ��У��ټ�������ˮ��Լ30 mL��, �ò���������������ʹ���Ͼ��ȣ��ڶ�����������ȴ�������ز�����ע������ƿ�У�����������30 mLˮϴ���ձ��ڱںͲ�����23�Σ�ϴ��Һ��ע������ƿ�������IJ�������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶���12 cm�������岽�����ý�ͷ�ιܼ�ˮ��ʹ��Һ��Һ��ǡ����̶������У���������.������ƿ�ǽ�����ҡ�ȣ����װƿ���档��������Һ����ȷ˳����BCAFED ����4�����ݹ�ʽ��c=n/V������������������ϡ��������ձ�δϴ�ӣ�ʹ���ʵ����ʵ���ƫС����Һ������䣬�����Һ�����ʵ���Ũ��ƫ�ͣ�������ƿ��ԭ����������ˮ������Һ�����ƹ�����Ӱ�죬�����ʵ����ʵ���Ũ�Ȳ��䣻������ʱ�۲�Һ�温�ӣ���Һ�����ƫС��������ʵ����ʵ���Ũ��ƫ�ߡ���5��������ʱ������ˮʱ�����˿̶ȣ���������������Һ����������ƿ��ת����Һʱ�й�Һ��������Һ���������ʵ����ʵ���ƫС������������Һ�����ʵ���Ũ�Ȳ��������������ƣ�������ҡ�����Һ���½��������������ơ�