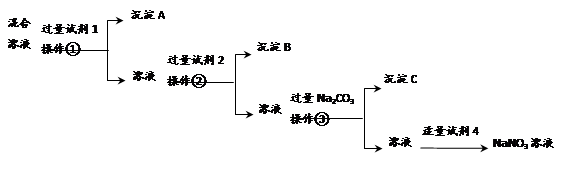题目内容
某铜矿石中铜元素含量较低,且含有铁、镁、钙等杂质。某小组在实验室中用浸出-萃取法制备硫酸铜:
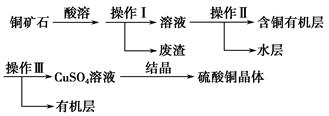
(1)操作Ⅰ为________。操作Ⅱ用到的玻璃仪器有烧杯、________。
(2)操作Ⅱ、操作Ⅲ的主要目的是________、富集铜元素。
(3)小组成员利用CuSO4溶液与Na2CO3溶液混合反应,制备环保型木材防腐剂Cu2(OH)2CO3悬浊液。多次实验发现所得蓝色悬浊液颜色略有差异,查阅资料表明,可能由于条件控制不同使其中混有较多Cu(OH)2或Cu4(OH)6SO4。
已知Cu(OH)2、Cu2(OH)2CO3,Cu4(OH)6SO4均难溶于水,可溶于酸;分解温度依次为80 ℃、200 ℃、300 ℃。
设计实验检验悬浊液成分,完成表中内容。
限选试剂:2 mol·L-1盐酸、1 mol·L-1 H2SO4、0.1 mol·L-1 NaOH溶液、0.1 mol·L-1 BaCl2溶液、蒸馏水。仪器和用品自选。
(4)上述实验需要100 mL 0.5 mol·L-1的CuSO4溶液,配制时需称取________g CuSO4·5H2O(相对分子质量:250)。

(1)操作Ⅰ为________。操作Ⅱ用到的玻璃仪器有烧杯、________。
(2)操作Ⅱ、操作Ⅲ的主要目的是________、富集铜元素。
(3)小组成员利用CuSO4溶液与Na2CO3溶液混合反应,制备环保型木材防腐剂Cu2(OH)2CO3悬浊液。多次实验发现所得蓝色悬浊液颜色略有差异,查阅资料表明,可能由于条件控制不同使其中混有较多Cu(OH)2或Cu4(OH)6SO4。
已知Cu(OH)2、Cu2(OH)2CO3,Cu4(OH)6SO4均难溶于水,可溶于酸;分解温度依次为80 ℃、200 ℃、300 ℃。
设计实验检验悬浊液成分,完成表中内容。
限选试剂:2 mol·L-1盐酸、1 mol·L-1 H2SO4、0.1 mol·L-1 NaOH溶液、0.1 mol·L-1 BaCl2溶液、蒸馏水。仪器和用品自选。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量悬浊液,过滤,充分洗涤后,取滤渣于试管中,______________________ | ____________,说明悬浊液中混有Cu4(OH)6SO4 |
| 步骤2:另取少量悬浊液于试管中,____________________ | ____________,说明悬浊液中混有Cu(OH)2 |
(4)上述实验需要100 mL 0.5 mol·L-1的CuSO4溶液,配制时需称取________g CuSO4·5H2O(相对分子质量:250)。
(1)过滤 分液漏斗
(2)除去杂质
(3)
(4)12.5
(2)除去杂质
(3)
| 实验步骤 | 预期现象和结论 |
| 加入过量2 mol·L-1盐酸,充分振荡,再滴加几滴0.1 mol·L-1 BaCl2溶液 | 有白色沉淀生成 |
| 将试管放入装有沸水的小烧杯中水浴加热一段时间,取出试管观察 | 试管中有黑色固体生成 |
(4)12.5
(1)由流程图可知操作Ⅰ是固、液分离,是过滤;操作Ⅱ是液液分离,且互不相溶,是分液,用到分液漏斗。(2)操作Ⅱ、Ⅲ的目的主要是除杂。
步骤1,由信息中三种物质均难溶于水,可溶于酸,故加入过量盐酸使之溶解,再用BaCl2溶液检验有无SO42—即可。步骤2,检验有无Cu(OH)2,可利用信息中三种物质分解温度不同,可在80 ℃时看有无分解产生CuO,若有,则有Cu(OH)2。(4)配制溶液需CuSO4的物质的量为0.1 L×0.5 mol·L-1=0.05 mol,即需要0.05 mol CuSO4·5H2O,其质量m=0.05 mol×250 g
·mol-1=12.5 g。
步骤1,由信息中三种物质均难溶于水,可溶于酸,故加入过量盐酸使之溶解,再用BaCl2溶液检验有无SO42—即可。步骤2,检验有无Cu(OH)2,可利用信息中三种物质分解温度不同,可在80 ℃时看有无分解产生CuO,若有,则有Cu(OH)2。(4)配制溶液需CuSO4的物质的量为0.1 L×0.5 mol·L-1=0.05 mol,即需要0.05 mol CuSO4·5H2O,其质量m=0.05 mol×250 g
·mol-1=12.5 g。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
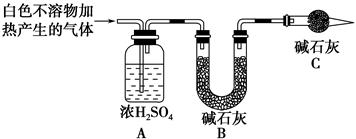
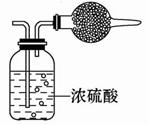
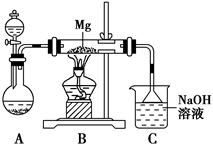
 2MgSO3+S;丙同学的推测是:3Mg+SO2
2MgSO3+S;丙同学的推测是:3Mg+SO2