题目内容
9.某元素的原子最外层有2个电子,关于该元素的推断一定正确的是( )| A. | 是金属元素 | B. | 是IIA族元素 | C. | 是非金属元素 | D. | 无法确定 |
分析 某元素的原子最外层有2个电子,可能为第ⅡA族元素或He或副族元素,以此来解答.
解答 解:某元素的原子最外层有2个电子,可能为第ⅡA族元素或He或副族元素,He为稀有气体元素,而第ⅡA族元素或副族元素均为金属元素,所以无法确定,
故选D.
点评 本题考查元素周期表的结构及应用,把握原子最外层有2个电子的元素可能为He及碱土金属元素为解答的关键,注意电子排布与元素位置的关系,题目难度不大.

练习册系列答案
相关题目
20.下列反应的离子方程式中,不正确的是( )
| A. | 碳酸氢钠溶液与少量石灰水反应:HCO3+Ca2++OH-=CaCO3↓+H2O | |
| B. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO+H20+CO2=CaCO3↓+2HClO | |
| C. | 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性:Ba2++2OH+2H++SO42-=BaSO4↓+2H2O | |
| D. | 碳酸氢钙溶液中加入盐酸:HCO3+H+=CO2↑+H20 |
17.某同学做元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:研究同周期元素性质的递变规律.
(2)实验用品:
试剂:金属钠,镁条、铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞试液等.
仪器:①小刀,②胶头滴管,③酒精灯,试管,试管夹,烧杯,镊子,玻璃片,砂纸,滤纸,火柴等.
(3)实验内容:实验②对应的现象:(填相应字母);实验⑥对应的离子反应是Al3++4OH-=AlO2-+2H2O
(4)实验所有实验步骤最终得出的结论是:金属性:Na>Mg>Al 非金属性:Cl>S.
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞试液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③用小刀切割一小块钠擦干煤油后放入滴有酚酞试液的装有冷水的烧杯中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将打磨后的镁投入装有稀盐酸的试管中 | D.反应不十分剧烈,产生无色气体 |
| ⑤将打磨后的铝投入装有稀盐酸的试管中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
(1)实验目的:研究同周期元素性质的递变规律.
(2)实验用品:
试剂:金属钠,镁条、铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞试液等.
仪器:①小刀,②胶头滴管,③酒精灯,试管,试管夹,烧杯,镊子,玻璃片,砂纸,滤纸,火柴等.
(3)实验内容:实验②对应的现象:(填相应字母);实验⑥对应的离子反应是Al3++4OH-=AlO2-+2H2O
(4)实验所有实验步骤最终得出的结论是:金属性:Na>Mg>Al 非金属性:Cl>S.
 中的两种基团组成的化合物,与NaOH溶液恰好完全发生反应,反应后所得产物中再通入二氧化碳,也能发生反应的物质可能是苯酚钠、碳酸钠.
中的两种基团组成的化合物,与NaOH溶液恰好完全发生反应,反应后所得产物中再通入二氧化碳,也能发生反应的物质可能是苯酚钠、碳酸钠. 已知在酸性条件下有以下反应:①2BrO3-+I2═2IO3-+Br2;②2IO3-+10Br-+12H+═I2+5Br2+6H2O.
已知在酸性条件下有以下反应:①2BrO3-+I2═2IO3-+Br2;②2IO3-+10Br-+12H+═I2+5Br2+6H2O.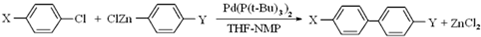
 .
.
 同分异构体的结构简式:
同分异构体的结构简式: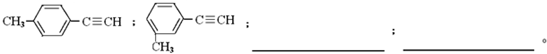
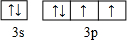 .
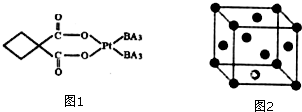
.
 图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,下层为四氯化碳,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:
图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,下层为四氯化碳,上层溶液为盐溶液,呈中性,请根据图示回答下列问题: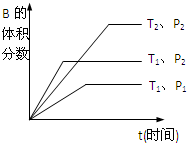 (1)已知某可逆反应mA(g)+nB(g)?qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空
(1)已知某可逆反应mA(g)+nB(g)?qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空