题目内容
【题目】室温下,单质A、B、C分别为固体、黄绿色气体与无色气体,在合适条件下,它们可以按下面的流程进行反应.又知E溶液是无色的.请回答: 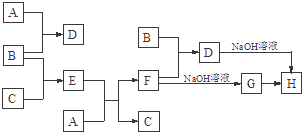
(1)写出E物质的化学式 .
(2)写出G→H的化学方程式 .
(3)写出B+F→D的离子方程式 .
【答案】
(1)HCl
(2)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(3)2Fe2++Cl2=2Fe3++2Cl﹣
【解析】解:由B为黄绿色气体且为单质,可知B为Cl2;由框图可知反应生成的固体D为固体单质A与Cl2反应生成的一种氯化物;反应生成的E为Cl2与气体单质C生成的一种可溶于水的氯化物,且E溶液和固体单质A又可以重新生成气体C和F,只有当C为H2 , F为一种氯化物时才能满足这一过程;而A与Cl2反应已生成了一种氯化物D,F又是一种氯化物,所以A为变价金属,应为Fe,所以A为Fe,B为Cl2 , C为H2 , D为FeCl3 , E为HCl,F为FeCl2 , G为Fe(OH)2 , H为Fe(OH)3 , (1)由上面的分析可知,E为HCl,所以答案是:E为HCl;(2)G→H为Fe(OH)2和O2反应生成Fe(OH)3的反应,反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3 , 所以答案是:4Fe(OH)2+O2+2H2O=4Fe(OH)3;(3)B+F→D的反应为Cl2和FeCl2生成FeCl3的反应,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl﹣ , 所以答案是:2Fe2++Cl2=2Fe3++2Cl﹣ .

 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案【题目】一定温度下,在容积为2L的密闭容器中发生反应CO(g)+H2O(g)CO2(g)+H2(g),部分数据见表(表中t2>t1),说法错误的是( )
反应时间/min | n(CO)/mol | n(H2O)/mol | n(CO2)/mol | n(H2)/mol |
0 | 1.20 | 0.60 | 0 | 0 |
t1 | 0.80 | |||
t2 | 0.20 |
A.反应在t1min末的速率为v(H2)=0.2/t molL﹣1min﹣1
B.平衡时水蒸气的转化率为66.67%
C.该温度下反应的平衡常数为1
D.其他条件不变,若起始时,n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时水蒸气的转化率为33.33%