��Ŀ����
����Ŀ����ʮ��������ѧ�����߶�̼�����������˹㷺������о���ȡ����һЩ��Ҫ�ɹ����ڸ��¸�ѹ��CO���м��ߵĻ�ѧ���ԣ�������ֵ��ʻ��ﷴӦ��
��1����ҵ�ϳ�����ˮ�����絽���ȵ�̿����ʵ��ú���������Ƶ�CO��H2�����÷�Ӧ�Ļ�ѧ����ʽ�� ��
��2������ú��������������̿�㽻�����������ˮ���������������Ŀ���� ����Ӧ���ɵ������ڼ��ȡ������������������ϳ�Һ��ȼ�ϼ״����÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3��һ�������£�CO��H2�ɺϳɼ��飬��Ӧ����ʽΪ��CO��g��+3H2��g��![]() CH4��g��+H2O ��g���������£��÷�Ӧ�ܹ��Է����е�ԭ���� ��
CH4��g��+H2O ��g���������£��÷�Ӧ�ܹ��Է����е�ԭ���� ��
��4��CO������ȼ�ϵ����ʹ�õĵ�����Dz�����Y2O3��ZrO2���壬���ڸ������ܴ���O2�����õ�������ĵ缫��ӦʽΪ ��
��5����ҵ�Ͽ�ͨ���״��ʻ�������ȡ�����������Ӧ����ʽΪ��
CH3OH��g����CO��g��![]() HCOOCH3��g�� ��H =��29.1 kJ��mol��1
HCOOCH3��g�� ��H =��29.1 kJ��mol��1
������Ա������Ӧ�������о��������о�������£�

�����ݷ�Ӧ��ϵ��ѹǿ�Լ״�ת���ʵ�Ӱ�첢�ۺϿ��������ɱ����أ���ҵ��ȡ�������Ӧѡ���ѹǿΪ ��
a��3.5��106Pa b��4.0��106Pa c��5.0��106Pa
��ʵ�ʹ�ҵ�����в��õ��¶��� ���������� ��
���𰸡���1��C��H2O![]() CO��H2
CO��H2
��2���ò���̿ȼ�����ṩ̿��ˮ������Ӧ����Ҫ������ CO + 2H2![]() CH3OH
CH3OH
��3�� ��H��0
��4��O2 + 4e��=2O2��
��5����b
��80�����¶ȵ���80������Ӧ���ʽ�С���¶ȸ���80�������¶Է�Ӧ����Ӱ���С���Ҹ÷�Ӧ���ȣ������¶�ƽ�������ƶ���ת���ʽ��͡�
��������
�����������1����ҵ�ϳ�����ˮ�����絽���ȵ�̿����ʵ��ú���������Ƶ�CO��H2�����÷�Ӧ�Ļ�ѧ����ʽ�ǣ�C��H2O![]() CO��H2��
CO��H2��
�ʴ�Ϊ��C��H2O![]() CO��H2��
CO��H2��
��2�����ݣ�1��ú��ˮ�����ķ�Ӧ����һ����̼������Ҫ���ȣ������������Ŀ�����ò���̿ȼ�գ���
��̿��ˮ������Ӧ����Ҫ��������һ����̼��������һ�������ºϳɼ״���ԭ��Ϊ��CO+2H2![]() CH3OH��
CH3OH��
�ʴ�Ϊ���ò���̿ȼ�գ��ṩ̿��ˮ������Ӧ����Ҫ��������CO+2H2![]() CH3OH��
CH3OH��
��3����CO��g��+3H2��g��![]() CH4��g��+H2O��g������Ӧ��S��0�������Է����е��ж����ݡ�H-T��S��0�����ԡ�H��0��
CH4��g��+H2O��g������Ӧ��S��0�������Է����е��ж����ݡ�H-T��S��0�����ԡ�H��0��
�ʴ�Ϊ���÷�Ӧ��H��0��
��4��COһ����ȼ�ϵ�أ�һ����̼�ڸ���ʧ���ӷ���������Ӧ��������Dz�����Y2O3��ZrO2���壬���ڸ������ܴ���O2���õ�ظ����ĵ缫��ӦʽΪ��CO-2e-+O2-=CO2�������缫��ӦΪ��O2 + 4e��=2O2����
�ʴ�Ϊ��O2 + 4e��=2O2����
��5���ٴӷ�Ӧѹǿ�Լ״�ת���ʵ�Ӱ�조Ч�ʡ�����ͼ����ת���ʱ仯������4.0��106Pa����b��ȷ��
�ʴ�Ϊ��b��
��ʵ�ʹ�ҵ�����в��õ��¶���80��C������ͼ������¶����¶ȵ���80������Ӧ���ʽ�С���¶ȸ���80�������¶Է�Ӧ����Ӱ���С���Ҹ÷�Ӧ���ȣ������¶�ƽ�������ƶ���ת���ʽ��͡�
�ʴ�Ϊ��80�棻�¶ȵ���80������Ӧ���ʽ�С���¶ȸ���80�������¶Է�Ӧ����Ӱ���С���Ҹ÷�Ӧ���ȣ������¶�ƽ�������ƶ���ת���ʽ��͡�

����Ŀ����������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷����ɵ�ص�ͭñ��Zn��Cu�ܺ���ԼΪ99%������ͭ���Ʊ�ZnO�IJ���ʵ�����������
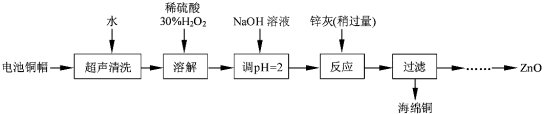
��1����д��ͭñ�ܽ������з�����Ӧ�Ļ�ѧ����ʽ ��
��ͭñ�ܽ���轫��Һ�й���H2O2��ȥ����ȥH2O2�ļ�㷽���� ��
��2��Ϊȷ������п������Ҫ�ɷ�ΪZn��ZnO������Ϊ��������������������ʵ������ⶨ��ȥH2O2����Һ��Cu2���ĺ�����ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2������Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�����pH=3��4���������KI����Na2S2O3����Һ�ζ����յ㡣���������е����ӷ���ʽ���£�
2Cu2����4I��=2CuI����ɫ������I2 I2��2![]() =2I����
=2I����![]()
���ζ�ѡ�õ�ָʾ��Ϊ ���ζ��յ�۲쵽������Ϊ ��
�����ζ�ǰ��Һ��H2O2û�г�������������Cu2���ĺ������� ���ƫ�ߡ�����ƫ�͡��������䡱����
��3����֪pH��11ʱZn��OH��2������NaOH��Һ����[Zn��OH��4]2�����±��г����������������������������pH����ʼ������pH����������Ũ��Ϊ1.0 mol��L��1������
Fe3�� | Fe2�� | Zn2�� | |
��ʼ������pH | 1.1 | 5.8 | 5.9 |
��ȫ������pH | 3.2 | 8.8 | 8.9 |
ʵ���п�ѡ�õ��Լ���30% H2O2��1.0 mol��L��1HNO3��1.0 mol��L��1 NaOH��
������ͭ������Һ�Ʊ�ZnO��ʵ�鲽������Ϊ��
�� ��
�� ��
�� ���ˣ�
�� ��
�� ���ˡ�ϴ�ӡ�����
�� 900�����ա�