题目内容
15.某溶液中可能有Fe3+、Mg2+、Na+、Ba2+、I-、Cl-、OH-、SO42-中的若干种,下列说法中正确的是( )| A. | 溶液中最多有4种离子 | B. | 若溶液有颜色,则一定没有OH-、I- | ||
| C. | 若溶液呈碱性,则一定含有Na+ | D. | 该溶液不可能溶解单质铜 |
分析 Fe3+、Mg2+均与OH-结合生成沉淀,Ba2+与SO42-结合生成沉淀,Fe3+与I-发生氧化还原反应,则溶液中可能含Fe3+、Mg2+、Na+、Cl-、SO42-,或Mg2+、Na+、Ba2+、I-、Cl-,或Na+、Ba2+、I-、Cl-、OH-,以此来解答.
解答 解:Fe3+、Mg2+均与OH-结合生成沉淀,Ba2+与SO42-结合生成沉淀,Fe3+与I-发生氧化还原反应,则溶液中可能含Fe3+、Mg2+、Na+、Cl-、SO42-,或Mg2+、Na+、Ba2+、I-、Cl-,或Na+、Ba2+、I-、Cl-、OH-,
A.由上述分析可知,溶液中可能存在5种离子,故A错误;
B.若溶液有颜色,则一定含Fe3+,可知一定没有OH-、I-,故B正确;
C.若溶液呈碱性,溶液一定含OH-,可含Na+,故C错误;
D.若含铁离子,则能溶解Cu,故D错误;
故选B.
点评 本题考查离子共存及常见离子之间的反应,为高频考点,把握常见离子之间的复分解反应、氧化还原反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
5.卤代烃是有机合成的重要中间体,某化学兴趣小组的同学查阅资料发现:加热l-丁醇、浓H2SO4和溴化钠混合物可以制备1-溴丁烷.
发生反应:CH3CH2CH2CH2OH+HBr→CH3CH2CH2CH2Br+H2O.还会有烯、醚等副产物生成.反应结束后将反应混合物蒸馏,分离得到1-溴丁烷,已知相关有机物的性质如下:
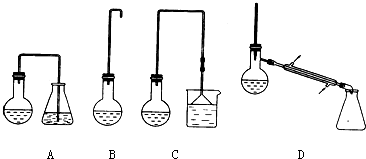
(1)制备1-溴丁烷的装置应选用上图中的C(填序号).反应加热时的温度不宜超过100℃,理由是防止1-溴丁烷因气化而逸出,影响产率且温度太高,浓硫酸氧化性增强,可能氧化溴化氢.
(2)制备操作中,加入的浓硫酸和溴化钠的作用是二者反应生成HBr.
(3)反应结束后,将反应混合物中1-溴丁烷分离出来,应选用的装置是D(填序号);该操作应控制的温度(t)范围是101.6℃≤t<117.25℃.
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是c.(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl.
发生反应:CH3CH2CH2CH2OH+HBr→CH3CH2CH2CH2Br+H2O.还会有烯、醚等副产物生成.反应结束后将反应混合物蒸馏,分离得到1-溴丁烷,已知相关有机物的性质如下:

| 熔点/℃ | 沸点/℃ | |
| 1-丁醇 | -89.53 | 117.25 |
| 1-溴丁烷 | -112.4 | 101.6 |
| 丁醚 | -95.3 | 142.4 |
| 1-丁烯 | -185.3 | -6.5 |
(2)制备操作中,加入的浓硫酸和溴化钠的作用是二者反应生成HBr.
(3)反应结束后,将反应混合物中1-溴丁烷分离出来,应选用的装置是D(填序号);该操作应控制的温度(t)范围是101.6℃≤t<117.25℃.
(4)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是c.(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl.
6.向浓度均为1mol/L的NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸,边加边振荡在整个过程中不可能发生的离子反应是( )
| A. | OH-+H+═H2O | B. | OH-+CO32-+2H+═HCO3-+H2O | ||
| C. | OH-+CO32-+3H+═CO2↑+2H2O | D. | 2OH-+CO32-+4H+═CO2↑+3H2O |
3.高温、催化剂条件下,某反应达到平衡,平衡常数K=$\frac{c(CO).c({H}_{2}O)}{c(C{O}_{2}).c({H}_{2})}$.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
| A. | 该反应的焓变为负值 | |
| B. | 2CO2(g)+2H2(g)?2CO(g)+2H2O(g)的平衡常数K1=K2 | |
| C. | 升高温度,正反应速率增大,逆反应速率减小,平衡正向移动 | |
| D. | 若恒容、恒温下充入CO,则K值变大 |
10.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 4g 氦气中含有的分子数为NA | |
| B. | 常温常压下,22.4LCl2中含有的分子数为NA | |
| C. | 1L1mol/LK2SO4溶液中含有的钾离子数为NA | |
| D. | 1mol钠原子中含有的电子数为NA |
20.下列碱性透明溶液中,能大量共存的离子组是( )
| A. | K+、Na+、MnO${\;}_{4}^{-}$、Cl- | B. | K+、Ag+、NO${\;}_{3}^{-}$、Cl- | ||
| C. | Ba2+、Na+、Cl-、SO${\;}_{4}^{2-}$ | D. | Na+、Cu2+、NO${\;}_{3}^{-}$、Cl- |
7.实验室中,要使明矾溶液中的Al3+全部沉淀出 来,适宜用的试剂是( )
| A. | NaOH溶液 | B. | 氨水 | C. | 盐酸 | D. | Ba(OH)2溶液 |
4.科学家发现了利用泪液来检测糖尿病的方法,其原理是用氯金酸钠(NaAuCl4)溶液与溶液中的葡萄糖发生反应生成纳米金单质颖粒(直径为20-60nm).下列有关说法错误的是( )
| A. | 氯金酸钠中金元素的化合价为+3 | |
| B. | 葡萄糖具有还原性 | |
| C. | 检测时,NaAuCl4发生氧化反应 | |
| D. | 纳米金单质颗粒分散在水中所得的分散系能产生丁达尔效应 |
5.下列说法正确的是( )
| A. | 固体氯化钠不导电,所以氯化钠是非电解质 | |
| B. | 氯化氢水溶液能导电,所以氯化氢是电解质 | |
| C. | 铜丝能导电,所以铜是电解质 | |
| D. | CO2的水溶液能导电,所以CO2是电解质 |