题目内容
【题目】POCl3常用作半导体掺杂剂及光导纤维原料,实验室制备POCl3并测定产品含量的实验过程如下:
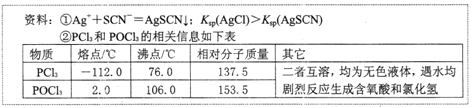
实验室制备POCl3。
采用氧气氧化液态PCl3法制取POCl3,实验装置(加热及夹持仪器略)如下:
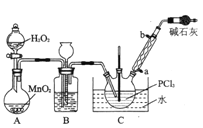
(1)B中所盛的试剂是______,干燥管的作用是________。
(2)装置C中生成POCl3的化学方程式为______________。
(3)装置B的作用除干燥O2外,还有______、_______。
(4)反应温度要控制在60~65℃,原因是________________。
测定POCl3产品的含量:
实验步骤:
①制备POCl3实验结束后,待三颈瓶中液体冷却至室温,准确称取16.73gPOC13产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解,将水解液配成100.00mL溶液。
②取10.00mL溶液于锥形瓶中,加入10.00mL3.2mol/LAgNO3标准溶液。
③加入少许硝基苯(硝基苯无色、难溶于水、密度比水大)。
④以Fe2(SO4)3溶液为指示剂,用0 .2mol/LKSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00mL KSCN溶液。
(5)步骤③中加入硝基苯的作用是__________。
(6)达到滴定终点时的现象为__________。
(7)产品中POCl3的百分含量为__________。
【答案】 浓硫酸,防止空气中的水蒸气进入三颈烧瓶 2PCl3+O2 2POCl3 平衡压强、观察O2的流速 温度过低,反应速度太慢 温度过高,PCl3易挥发,利用率低 防止在滴加KSCN溶液时,将AgCl沉淀转化为AgSCN沉淀 溶液由无色变为红色,且半分钟内不褪色 91.8%
【解析】(1)A中产生氧气,则B中所盛的试剂是干燥氧气,应该是浓硫酸;POCl3遇水水解,因此干燥管的作用是防止空气中的水蒸气进入三颈烧瓶。(2)氧气和三氯化磷反应生成POCl3,反应的化学方程式为2PCl3+O2=2POCl3。(3)装置B中有长颈漏斗,因此B的作用除干燥O2外,还有平衡压强、观察O2的流速。(4)反应温度要控制在60~65℃,原因是温度过低,反应速度太慢,而温度过高,PCl3易挥发,利用率低。(5)已知:Ksp(AgCl)>Ksp(AgSCN),则AgSCN沉淀的溶解度比AgCl小,可加入硝基苯用力摇动,使AgCl沉淀表面被有机物覆盖,避免在滴加KSCN时,将AgCl沉淀转化为AgSCN沉淀;(6)用c molL-1KSCN溶液滴定过量Ag+至终点,当滴定达到终点时KSCN过量,Fe3+与SCN-反应溶液会变红色,半分钟内不褪色,即可确定滴定终点,因此达到滴定终点时的现象为溶液由无色变为红色,且半分钟内不褪色。(7)剩余硝酸银的物质的量是0.2mol/L×0.01L=0.002mol,因此与氯离子反应的硝酸银是0.032mol-0.002mol=0.03mol,则原溶液中氯离子的物质的量是0.03mol×100mL/10mL=0.3mol,则POCl3是0.1mol,质量是15.35g,则产品中POCl3的百分含量为15.35g/16.73g×100%=91.8%。

【题目】草酸钴用途广泛,可用于指示剂和催化剂制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:
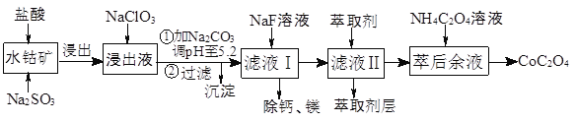
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的目的是将_____________还原(填离子符号)以便固体溶解。该步反应的离子方程式为 (写一个)。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,氯元素被还原为最低价。该反应的离子方程式为 。
(3)利用平衡移动原理分析:加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是 。
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液Ⅱ中加入萃取剂的作用是 ;使用萃取剂适宜的pH=____(填序号)左右:
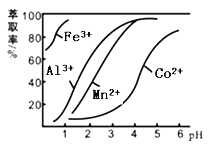
A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)= 。