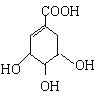
题目内容
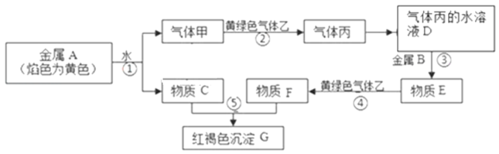
【题目】现有黄绿色气体乙为Cl2,金属单质A、B和气体甲、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中某些反应的产物及条件没有全部标出)
(1)丙的化学式为___;
(2)F溶液常用于腐蚀印刷电路板,请写出相关的离子方程式:___;
(3)为鉴定B单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是___;
a.碘水 b.氯水 c.Na2SO3溶液 d.KSCN溶液
(4)C溶液中加入过量的Al2O3固体的离子反应方程式为___;向反应后的溶液中通入过量的CO2气体的离子反应方程式为___。
【答案】HCl 2Fe3++Cu=2Fe2++Cu2+ bd Al2O3+2OH-=2AlO2-+H2O AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
【解析】
金属A的焰色反应为黄色,则A为Na,A与水反应生成气体甲为H2,物质C为NaOH;C与F反应生产线红褐色沉淀G应为Fe(OH)3,可知F含有Fe3+;黄绿色气体乙为Cl2,氯气与氢气反应生成气体丙为HCl,HCl的水溶液D为盐酸,由转化关系可知金属B为Fe、E为FeCl2、F为FeCl3。
(1)根据分析可知丙为HCl;
(2)Fe3+具有强氧化性可以氧化铜单质生成Cu2+,离子方程式为2Fe3++Cu=2Fe2++Cu2+;
(3)金属B为Fe,与盐酸反应可以生成Fe2+,亚铁离子可以被氯气氧化成Fe3+,Fe3+可以与KSCN溶液作用显血红色,所以取上层清液后需再加入的试剂为b、d;
(4)NaOH溶液中加入过量的Al2O3固体的离子反应方程式为:Al2O3+2OH-=2AlO2-+H2O;向反应后的溶液中通入过量二氧化碳,由于碳酸不能溶解氢氧化铝,所以最终产物为氢氧化铝沉淀和碳酸氢钠,离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】将E(g)和F(g)加入密闭容器中,在一定条件下发生反应:E(s)+4F(g)G(g),已知该反应的平衡常数如表所示。下列说法正确的是( )
温度/℃ | 25 | 80 | 230 |
平衡常数/(L3·mol-3) | 5×104 | 2 | 1.9×10-5 |
A.上述反应是熵增反应
B.25 ℃时,反应G(g)E(s)+4F(g)的平衡常数是0.5 mol3·L-3
C.在80 ℃时,测得某时刻,F、G的浓度均为0.5 mol·L-1,则此时v正>v逆
D.恒温恒容下,向容器中再充入少量G(g),达新平衡时,G的体积百分含量将增大