题目内容
【题目】下列叙述中不正确的是( )(已知Ksp(AgCl)=4.0×10-10,Ksp(AgBr)=4.9×10-13,Ksp(Ag2CrO4)=2.0×10-12)
A.0.l mol·L-1 NH4HS溶液中有:c(NH4+)+c(NH3·H2O)>c(HS-)+c(S2-)
B.将AgCl和AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,AgCl沉淀质量大于AgBr沉淀
C.向浓度均为1×10-3 mol/L的KCl和K2CrO4混合液中滴加1×10-3 mol/L AgNO3溶液,先生成AgCl沉淀
D.常温下,pH=4.75、浓度均为0.l mol/L的CH3COOH、CH3COONa混合溶液:c(CH3COO-)+c(OH-) = c(CH3COOH)+c(H+)
【答案】D
【解析】
A选项,根据物料守恒,0.l mol·L-1 NH4HS溶液中有:c(NH4+)+c(NH3·H2O) = c(HS-)+c(S2-) +c(H2S),因此有c(NH4+)+c(NH3·H2O)>c(HS-)+c(S2-),故A正确;
B选项,AgCl饱和溶液中c(Cl-)=![]() mol/L=2×10-5mol/L,AgBr饱和溶液中c(Br-)=
mol/L=2×10-5mol/L,AgBr饱和溶液中c(Br-)=![]() mol/L=7×10-7mol/L,AgCl饱和溶液中Cl-浓度远大于AgBr饱和溶液中Br-浓度,将AgCl和AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,则原溶液中的氯离子和溴离子沉淀,AgCl物质的量远远大于AgBr,因此AgCl沉淀质量大于AgBr沉淀,故B正确;
mol/L=7×10-7mol/L,AgCl饱和溶液中Cl-浓度远大于AgBr饱和溶液中Br-浓度,将AgCl和AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,则原溶液中的氯离子和溴离子沉淀,AgCl物质的量远远大于AgBr,因此AgCl沉淀质量大于AgBr沉淀,故B正确;
C选项,浓度均为1×10-3 mol/L的KCl和K2CrO4混合液中,氯离子沉淀需要的银离子浓度为![]() mol/L,CrO42-沉淀需要的银离子浓度为
mol/L,CrO42-沉淀需要的银离子浓度为![]() mol/L=
mol/L=![]() ×10-5mol/L>4×10-7mol/L,向混和溶液中滴加1×10-3 mol/L AgNO3溶液,先生成AgCl沉淀,故C正确;
×10-5mol/L>4×10-7mol/L,向混和溶液中滴加1×10-3 mol/L AgNO3溶液,先生成AgCl沉淀,故C正确;
D选项,常温下,pH=4.75浓度均为0.l mol/L的CH3COOH、CH3COONa混合溶液,根据电荷守恒得到c(CH3COO-)+c(OH-) = c(Na+)+c(H+),根据物料守恒得到c(CH3COO-)+c(CH3COOH) =2c(Na+),因此得到c(CH3COO-)+2c(OH-) = c(CH3COOH)+2c(H+),故D错误;
综上所述,答案为D。

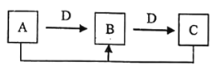
【题目】有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装置 |
|
|
部分实验现象 | a极质量减小b极质量增加 | b极有气泡产生c极无变化 |
实验装置 |
|
|
部分实验现象 | d极溶解c极有气泡产生 | 电流从a极流向d极 |
由此判断这四种金属的活动性顺序是( )
A. a>b>c>dB. d>a>b>cC. b>c>d>aD. a>b>d>c
【题目】环境问题越来越受到人们的重视,“绿水青山就是金山银山”的理念已被人们认同。运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染具有重要意义。回答下列问题:
(1)亚硝酰氯(Cl—N=O)气体是有机合成中的重要试剂,它可由Cl2和NO在通常条件下反应制得,该反应的热化学方程式为______________________。相关化学键的键能如下表所示:
化学键 | Cl—Cl | N≡O(NO气体) | Cl—N | N=O |
键能/(kJ·mol-1) | 243 | 630 | 200 | 607 |
(2)有人设想采用下列方法减少SO2、NO2对环境的污染:用CH4还原SO2,从产物中分离出一种含硫质量分数约为94%的化合物,并用这种化合物来还原NO2。这种含硫化合物和NO2反应的化学方程式为______________________。
(3)用NaOH溶液吸收SO2也是减少大气污染的一种有效方法。25℃时,将一定量的SO2通入到NaOH溶液中,两者完全反应,若溶液中![]() ,则该混合溶液的pH=___________(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。
,则该混合溶液的pH=___________(25℃时,H2SO3的电离平衡常数Ka1=1.0×10-2,K a2=1.0×10-7)。