题目内容
【题目】可溶性钡盐有毒,医院中常用硫酸钡这种钡盐(俗称钡餐)作为内服造影剂。医院抢救钡离子中毒患者时除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:Ksp(BaCO3)=5.1×10-9;Ksp(BaSO4)=1.1×10-10。下列推断正确的是
A.BaCO3的溶度积常数表达式为 Ksp(BaCO3)= n(Ba2+)·n(CO32-)
B.可用2%~5%的Na2SO4溶液给钡离子中毒患者洗胃
C.若误服含c(Ba2+)=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
D.不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4)
【答案】B
【解析】
因胃酸可与CO32反应生成水和二氧化碳,使CO32浓度降低,从而使平衡BaCO3(s)Ba2+(aq)+CO32(aq) 向溶解方向移动,则BaCO3溶于胃酸,而硫酸钡不溶于酸,结合溶度积解答该题。
A.溶度积常数为离子浓度幂之积,BaCO3的溶度积常数表达式为Ksp(BaCO3)=c(Ba2+)·c(CO32-),故A错误;
B.根据公式c=![]() 得,2%~5%的Na2SO4溶液中Na2SO4的物质的量浓度为0.13mol/L~0.33mol/L,用0.13mol/L~0.33mol/L的Na2SO4溶液给钡离子中毒患者洗胃,反应后c(Ba2+)=
得,2%~5%的Na2SO4溶液中Na2SO4的物质的量浓度为0.13mol/L~0.33mol/L,用0.13mol/L~0.33mol/L的Na2SO4溶液给钡离子中毒患者洗胃,反应后c(Ba2+)=![]() mol/L~
mol/L~![]() mol/L,浓度很小,可起到解毒的作用,故B正确;
mol/L,浓度很小,可起到解毒的作用,故B正确;
C.c(Ba2+)=1.0×105 molL1的溶液钡离子浓度很小,不会引起钡离子中毒,故C错误;
D.因胃酸可与CO32反应生成水和二氧化碳,使CO32浓度降低,从而使平衡BaCO3(s)Ba2+(aq)+CO32(aq) 向溶解方向移动,使Ba2+浓度增大,Ba2+有毒,与Ksp大小无关,故D错误;
故答案选B。

【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(含25%BeO、71%CuS、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如图:
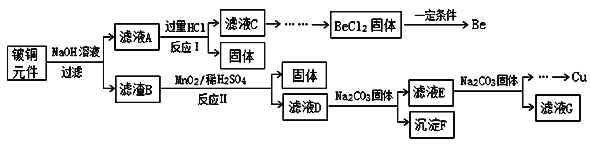
已知:I、铍、铝元素化学性质相似;
Ⅱ、常温下部分难溶物的溶度积常数如表:
难溶物 | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
溶度积常数(Ksp) | 2.2×10-20 | 4.0×10-38 | 2.1×10-13 |
(1)滤液A的主要成分除NaOH、Na2BeO2外,还有___________(填化学式),写出反应I中Na2BeO2与过量盐酸反应的离子方程式:________。
(2)滤液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,最合理的实验步骤顺序为_______(填字母)
a.加入过量的氨水 b.通入过量的CO2 c.加入过量的NaOH d.加入适量的HCl e.洗涤 f.过滤
(3)MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应Ⅱ中CuS发生反应的化学方程式:___________。若用浓HNO3溶解金属硫化物,缺点是_______(任写一条)。
(4)滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=8.0×10-3mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入Na2CO3溶液调节pH可将其转变成氢氧化物依次分离,首先沉淀的是_______(填离子符号);为使铜离子开始沉淀,常温下应调节溶液的pH大于______。
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如表:下列说法错误的是:( )
物质 | X | Y | Z |
初始浓度/ | 0.1 | 0.2 | 0 |
平衡浓度/ | 0.05 | 0.05 | 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.改变温度可以改变此反应的平衡常数
D.增压使平衡向生成Z的方向移动,平衡常数增大
【题目】下列实验操作、理象和结论均正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 向某溶液中加入NaOH 溶液,并用湿润的红色石蕊试纸检验 | 试纸没有变蓝 | 原溶液中没有有NH4+ |
B | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
C | 向某溶液中滴加氯水后,再加KSCN溶液 | 溶液变红 | 原溶液中一定有Fe2+ |
D | 向某无色溶液中滴加BaCl2溶液 | 产生白色沉淀 | 该无色溶液中一定含有SO42- |
A. A B. B C. C D. D