题目内容
【题目】某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。
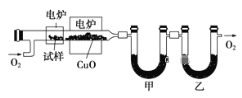
步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收.2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水;
步骤二:通过仪器分析得知X的相对分子质量为106;
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3 (如图Ⅰ)
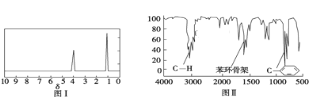
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ,试回答:
(1)步骤二中的仪器分析方法称为___________。
(2)X的分子式为___________;(写出计算过程)X的结构简式为___________;
【答案】质谱法 烃X的物质的量为2.12g÷106g/mol=0.02mol,生成二氧化碳为7.04g÷44g/mol=0.16mol,生成水为1.8g÷18g/mol=0.1mol,则分子中N(C)=0.16mol÷0.02mol=8、N(H)=0.1mol×2÷0.02mol=10,故X的分子式为C8H10 ![]()
【解析】
烃X的物质的量为2.12g÷106g/mol=0.02mol,生成二氧化碳为7.04g÷44g/mol=0.16mol,生成水为1.8g÷18g/mol=0.1mol,则分子中N(C)=0.16mol÷0.02mol=8、N(H)=0.1mol×2÷0.02mol=10,故X的分子式为C8H10,X的红外光谱测定含有苯环,属于苯的同系物,而1H核磁共振谱有2个峰,其面积之比为2:3,则X为![]() 。
。
(1)通过仪器分析得知相对分子质量的方法为质谱法,故答案为:质谱法;
(2)分子中N(C)=0.16mol÷0.02mol=8、N(H)=0.1mol×2÷0.02mol=10,故X的分子式为C8H10,X的红外光谱测定含有苯环,属于苯的同系物,而1H核磁共振谱有2个峰,其面积之比为2:3,则X为![]() 。故答案为:C8H10 ,
。故答案为:C8H10 , ![]() 。
。