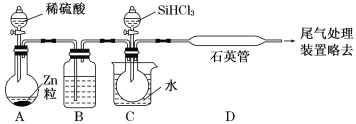
题目内容
【题目】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用CsCO3,XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7,的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为__;第一电离能I1(Si)__I1(Ge)(填![]() 或
或![]() )。
)。
(2)基态Ge原子核外电子排布式为__;SiO2,GeO2具有类似的晶体结构,其中熔点较高的是__,原因是__。
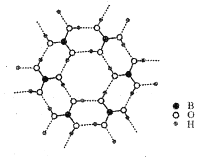
(3)如图为H3BO3晶体的片层结构,其中B的杂化方式为__;硼酸在热水中比在冷水中溶解度显著增大的主要原因是__。
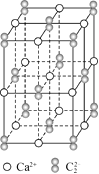
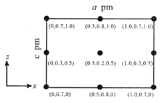
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7,属正交晶系(长方体形),晶胞参数为apm、bpm和cpm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为__;CsSiB3O7的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为__g·cm-3(用代数式表示)。
【答案】O>C>Si > 1s22s22p63s23p63d104s24p2(或[Ar]3d104s24p2) SiO2 二者均为原子晶体,Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高 sp2 热水破坏了硼酸晶体中的氢键,并且硼酸分子与水形成分子间氢键,使溶解度增大 4 ![]()
【解析】
⑴电负性的变化规律为同周期从左向右逐渐增大,同主族由上至下逐渐减小,第一电离能的变化规律为同族元素由上至下逐渐减小。
⑵SiO2、GeO2为同类型晶体结构,即为原子晶体,Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高。
⑶B原子最外层有3个电子,与3个-OH形成3个共价键,即可得杂化方式,热水破坏了硼酸晶体中的氢键,并且硼酸分子与水形成分子间氢键,使溶解度增大。
⑷先分析得出Cs的个数,再根据公式计算密度。
⑴电负性的变化规律为同周期从左向右逐渐增大,同主族由上至下逐渐减小,所以电负性O>C>Si;第一电离能的变化规律为同族元素由上至下逐渐减小,因此I1(Si)>I1(Ge),故答案为:O>C>Si;>。
⑵Ge原子位于第四周期IVA族,因此原子核外电子排布式为1s22s22p63s23p63d104s24p2(或[Ar]3d104s24p2);SiO2、GeO2均为原子晶体,Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高,故答案为:1s22s22p63s23p63d104s24p2(或[Ar]3d104s24p2);SiO2;Ge原子半径大于Si,Si-O键长小于Ge-O键长,SiO2键能更大,熔点更高。
⑶B原子最外层有3个电子,与3个-OH形成3个共价键,因此为sp2杂化;热水破坏了硼酸晶体中的氢键,并且硼酸分子与水形成分子间氢键,使溶解度增大;故答案为:p2;热水破坏了硼酸晶体中的氢键,并且硼酸分子与水形成分子间氢键,使溶解度增大。
⑷原子分数坐标为(0.5,0.2,0.5)的Cs原子位于晶胞体内,原子分数坐标为(0,0.3,0.5)及(1.0,0.3,0.5)的Cs原子位于晶胞的yz面上,原子分数坐标为(0.5,0.8,1.0)及(0.5,0.8,0)的Cs原子位于晶胞xy面上,原子分数坐标为(0,0.7,1.0)及(1.0,0.7,1.0)(0,0.7,0)及(1.0,0.7,0)的Cs原子位于晶胞平行于y轴的棱上,利用均摊法可计算该晶胞中共含Cs原子4个;带入晶胞密度求算公式可得:
ρ=![]() g·cm-3,故答案为:4;
g·cm-3,故答案为:4;![]() 。
。

【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
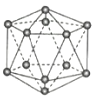
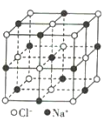
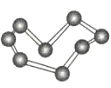
晶体硼(其每个结构单元中有12个B原子) | NaCl | S8 | HCN | |
结构模型示意图 |
|
|
|
|
备注 | 熔点2573K | —— | 易溶于CS2 | —— |
A.晶体硼属于原子晶体,结构单元中含有30个B-B键,含20个正三角形
B.NaCl晶体中每个Na+周围距离最近且相等的Na+有6个
C.S8分子中的共价键为非极性键
D.HCN分子中含有2个σ键,2个π键