题目内容
4.氧原子最外层电子数是其K层电子数的3倍;硫原子次外层电子数与M层电子数之差为2;氯原子核外电子由低到高分别占据了3层.分析 根据核外电子排布规律可知,氧原子的每一层上的电子数分别2、6,硫原子每一层上的电子数分别2、8、6,硫原子每一层上的电子数分别2、8、7,据此解答.
解答 解:氧原子的每一层上的电子数分别2、6,则最外层电子数是其K层电子数的3倍;
硫原子每一层上的电子数分别2、8、6,则次外层电子数与M层电子数之差为2;
硫原子每一层上的电子数分别2、8、7,则核外电子由低到高分别占据了3层;
故答案为:3;2;3.
点评 本题主要考查原子核外电子排布知识,难度不大,注意基础知识的积累与运用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.下列反应的离子方程式,书写错误的是( )
| A. | 钠放入水中:Na+2H+=2Na++H2↑ | |
| B. | 铜粉放入硝酸银溶液里:Cu+2Ag+=Cu2++2Ag | |
| C. | 氢氧化钡跟硫酸铜溶液的反应:Ba2++2OH-+Cu2++SO2-4=BaSO4↓+Cu(OH)2↓ | |
| D. | 氯化铁溶液中滴加硝酸银溶液:Cl-+Ag+=AgCl↓ |
12.为测定空气中CO2含量,做下述实验:
(1)为配置标准溶液,请选取必需的一组仪器B;
①托盘天平 ②容量瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒
A、①②⑤⑥B、②④⑤⑥⑦C、①②⑥⑦D、②④⑤⑥
(2)滴定操作时,左手控制酸式滴定管活塞,眼睛注视液滴下滴速度和锥形瓶中溶液颜色的变化;
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤.需过滤的原因是除去BaCO3沉淀,使滤液只含Ba(OH)2,以保证实验成功;
(4)由实验数据算出空气中CO2的体积分数为0.025%;
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即更换溶液,进行第二次滴定,导致实验数据值(填偏高、偏低或无影响)偏高.
| 配0.1mol/L的标准盐酸和0.01mol•L-1的标准盐酸 | → | 用0.1mol•L-1的标准盐酸滴定未知Ba(OH)2溶液10mL用去盐酸19.60mL | → | 用Ba(OH)2溶液吸收空气中的CO2 | → | 过 滤 | → | 取滤液20mL,用0.01mol•L-1的盐酸滴定用去盐酸34.8mL |
①托盘天平 ②容量瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥胶头滴管 ⑦玻璃棒
A、①②⑤⑥B、②④⑤⑥⑦C、①②⑥⑦D、②④⑤⑥
(2)滴定操作时,左手控制酸式滴定管活塞,眼睛注视液滴下滴速度和锥形瓶中溶液颜色的变化;
(3)取上述Ba(OH)2溶液10mL放入100mL容量瓶中,加水稀释至刻度,把稀释后的溶液放入密闭容器,并引入10L空气,振荡,过滤.需过滤的原因是除去BaCO3沉淀,使滤液只含Ba(OH)2,以保证实验成功;
(4)由实验数据算出空气中CO2的体积分数为0.025%;
(5)本实验中,若第一次滴定时使用的酸式滴定管未经处理,即更换溶液,进行第二次滴定,导致实验数据值(填偏高、偏低或无影响)偏高.
19.正己烷是优良的有机溶剂,其球棍模型为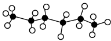 ,X是它的一种同分异构体,且X分子的主链上含有4个碳原子,下列有关说法中正确的是( )
,X是它的一种同分异构体,且X分子的主链上含有4个碳原子,下列有关说法中正确的是( )
 ,X是它的一种同分异构体,且X分子的主链上含有4个碳原子,下列有关说法中正确的是( )
,X是它的一种同分异构体,且X分子的主链上含有4个碳原子,下列有关说法中正确的是( )| A. | X分子中可能含有三个甲基 | |
| B. | X的一氯代物一定有三种 | |
| C. | 在催化剂存在下加热正己烷时可得到丁烷、丙烷、乙烯、丙烯等物质 | |
| D. | X能使溴的四氯化碳溶液褪色 |
3.锂被誉为“金属味精”,以LiCoO2为正极材料的锂离子电池已被广泛用作便携式电源.工业上常以β锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂.其中一种工艺流程如下: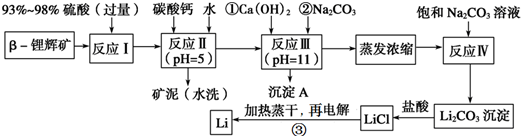
已知:部分金属氢氧化物开始沉淀和完全沉淀时的pH:
请回答下列问题:
(1)写出反应Ⅰ中有电子转移的化学方程式2FeO+4H2SO4=Fe2(SO4)3+SO2↑+H2O;
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4,控制pH,使Fe3+、Al3+完全沉淀;
(3)有同学认为在反应Ⅲ中只需加入碳酸钠溶液也能达成该步骤的目的,请阐述你的观点和理由不能,离子不能完全除去;
(4)上述流程蒸发浓缩环节,若在实验室进行该操作,当蒸发浓缩至晶体膜出现时,就可停止该操作.
(5)Li与Mg、Be与Al、B与Si这三对元素在周期表中处于对角线位置,相应的两元素及其化合物的性质有许多相似之处.这种相似性称为对角线规则.步骤③中电解时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
(6)请设计一种从水洗后的矿泥中分离出Al2O3的流程:矿泥$→_{过滤}^{足量NaOH}$滤液$\stackrel{足量二氧化碳}{→}$氢氧化铝$\stackrel{△}{→}$Al2O3(流程常用的表示方式为:A$→_{实验操作}^{反应试剂}$B…$→_{实验操作}^{反应试剂}$目标产物).

已知:部分金属氢氧化物开始沉淀和完全沉淀时的pH:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
(1)写出反应Ⅰ中有电子转移的化学方程式2FeO+4H2SO4=Fe2(SO4)3+SO2↑+H2O;
(2)反应Ⅱ加入碳酸钙的作用是除去反应Ⅰ中过量的H2SO4,控制pH,使Fe3+、Al3+完全沉淀;
(3)有同学认为在反应Ⅲ中只需加入碳酸钠溶液也能达成该步骤的目的,请阐述你的观点和理由不能,离子不能完全除去;
(4)上述流程蒸发浓缩环节,若在实验室进行该操作,当蒸发浓缩至晶体膜出现时,就可停止该操作.
(5)Li与Mg、Be与Al、B与Si这三对元素在周期表中处于对角线位置,相应的两元素及其化合物的性质有许多相似之处.这种相似性称为对角线规则.步骤③中电解时,阳极产生的氯气中会混有少量氧气,原因是加热蒸干LiCl溶液时,LiCl有少量水解生成LiOH,受热分解生成Li2O,电解时产生O2.
(6)请设计一种从水洗后的矿泥中分离出Al2O3的流程:矿泥$→_{过滤}^{足量NaOH}$滤液$\stackrel{足量二氧化碳}{→}$氢氧化铝$\stackrel{△}{→}$Al2O3(流程常用的表示方式为:A$→_{实验操作}^{反应试剂}$B…$→_{实验操作}^{反应试剂}$目标产物).
20.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号,下同),原子结构示意图为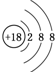 .元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.
.元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是: .
.
(3)用电子式表示元素④与⑥的化合物的形成过程: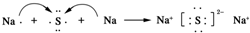 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.
(4)表示①与⑦的化合物的电子式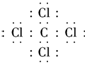 ,该化合物是由极性(填“极性”、“非极性”)键形成的.
,该化合物是由极性(填“极性”、“非极性”)键形成的.
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
(6)元素③的氢化物的结构式为H-O-H;该氢化物常温下和元素⑦的单质反应的化学方程式为Cl2+H2O═HClO+HCl.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.
.元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是:
 .
.(3)用电子式表示元素④与⑥的化合物的形成过程:
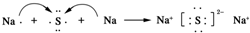 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.(4)表示①与⑦的化合物的电子式
 ,该化合物是由极性(填“极性”、“非极性”)键形成的.
,该化合物是由极性(填“极性”、“非极性”)键形成的.(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是S2->Cl->O2-.
(6)元素③的氢化物的结构式为H-O-H;该氢化物常温下和元素⑦的单质反应的化学方程式为Cl2+H2O═HClO+HCl.
1.已知在25℃、1.013×105Pa条件下,1molH2在氧气中完全燃烧后放出286KJ热量,1mol水蒸气转化为液态水放出热量为44KJ.其他的相关数据如下表:
则表中a为( )
| 物质 | H2(g) | O2(g) | H2O(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/KJ | 436 | 496 | a |
| A. | 463 | B. | 260 | C. | 926 | D. | 970 |
 如图是元素周期表中几种短周期主族元素原子半径随原子序数的变化.
如图是元素周期表中几种短周期主族元素原子半径随原子序数的变化.