题目内容
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。

回答下列问题:
(1)反应的△H_______0(填“大于”或“小于”) ;100℃时,体系中各物质浓度随时间变化如上图所示。在0-60s时段,反应速率v(N2O4)为______mol·L-1·s-1;反应的平衡常数K1为________。
(2) 100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,经10s又达到平衡。
a: T______100℃ (填“大于”或“小于”) ,判断理是_______
b:计算温度T时反应的平衡常数K2(要求写出计算过程)__________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向______(填“正反应”或“逆反应”)方向移动,判断理由是__________
【答案】 大于 0.001 0.36 大于 反应正方向吸热,反应向吸热方向进行,故温度升高 平衡时c(NO2)=0.120mol·L-1+0.0020mol·L-1·s-1×10s×2=0.16mol·L-1,c(N2O4)=0.040mol·L-1-0.0020mol·L-1·s-1×10s=0.020mol·L-1,K2=(0.16mol/L)2/0.020mol/L=1.3mol/L 逆反应 对气体分子数增大的反应,增大压强平衡向逆反应方向移动
【解析】试题(1)随温度升高,混合气体的颜色变深,所以平衡正向移动,焓变大于0;v(N2O4)=(0.1-0.04)÷60="0.0010" molL-1s-1;平衡常数K1为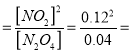 0.36 mol·L-1;(2)a:改变反应温度为T,c(N2O4)降低,平衡正向移动,所以改变条件为升温;T大于100℃;改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10s又达到平衡,所以c(N2O4)=0.04-0.002×10="0.02" mol·L-1;c(NO2)=(0.1-0.02)×2="0.16" mol·L-1;K2=" (0.16" mol·L-1)2/(0.020 mol·L-1) ="1.3" mol·L-1;(3)对气体分子数增大的反应,增大压强平衡向逆反应方向移动,温度T时反应达平衡后,将反应容器的容积减少一半,压强增大,所以平衡向逆反应方向移动。
0.36 mol·L-1;(2)a:改变反应温度为T,c(N2O4)降低,平衡正向移动,所以改变条件为升温;T大于100℃;改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10s又达到平衡,所以c(N2O4)=0.04-0.002×10="0.02" mol·L-1;c(NO2)=(0.1-0.02)×2="0.16" mol·L-1;K2=" (0.16" mol·L-1)2/(0.020 mol·L-1) ="1.3" mol·L-1;(3)对气体分子数增大的反应,增大压强平衡向逆反应方向移动,温度T时反应达平衡后,将反应容器的容积减少一半,压强增大,所以平衡向逆反应方向移动。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案