题目内容
标准状况下,一体积水能溶解700体积氨气,得到密度为0.9g/mL的氨水,计算此氨水的物质的量浓度为 。
18.37 mol/L
解析试题分析:氨气溶解于水得到氨水,先计算溶质的质量分数:(溶质的质量÷溶液的质量)×100%={(气体的体积÷气体摩尔体积)×摩尔质量}∕{(1000+(气体的体积÷气体摩尔体积)×摩尔质量})×100%
;利用物质的量浓度与质量分数的换算式C=(密度×1000×质量分数)÷摩尔质量即可计算出溶液的物质的量浓度。计算过程略。,
考点:考查质量与气体体积的相互关系及质量分数、物质的量浓度的计算与换算关系等的知识。

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
某草酸盐晶体KxFey(C2O4)z?wH2O中铁为+3价,草酸根为-2价,且知x+y+z=7。取该晶体做了以下实验:
① 取4.910g晶体在不同温度下加热至恒重,所得固体的化学式和质量如下表:
| | 120℃ | 300℃ | 480℃ |
| 化学式 | KxFey(C2O4)z | KxFeyO(C2O4)z-1 | KxFeyO2(C2O4)z-2 |
| 质量 | 4.370g | 3.650g | 2.930 g |
② 另取4.910g晶体,经过加酸溶解、加足量碱沉淀、灼烧至恒重,铁元素全部转化为Fe2O3,质量为0.800g。
(1)计算得出草酸盐晶体中结晶水的质量分数为 (保留三位小数);
(2)R的化学式为 ;
(3)草酸盐晶体的摩尔质量为 ;
(4)试通过计算,确定草酸盐晶体的化学式。
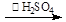
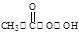 (过氧乙酸)+H2O
(过氧乙酸)+H2O