题目内容
【题目】白磷在过量氢氧化钾溶液中可以发生反应:P4+3KOH+3H2O = PH3↑+3KH2PO2。若用NA表示阿伏加德罗常数的值。下列说法错误的是
A.3.1 g白磷所含共价键的数目为0.15NA
B.KH2PO2为正盐,且10.4 g该固体物质中含离子数目为0.2NA
C.2.8 g KOH参加反应转移的电子数为0.05NA
D.室温下,10 mL pH=11的KOH溶液稀释100倍,水电离出的OH-的数目约为10-5NA
【答案】D
【解析】
A.白磷分子为正四面体形,4个磷原子位于4个顶点,所以一个白磷分子中含有6个共价键,则3.1 g白磷即0.025 P4含共价键0.15mol,即0.15NA,故A正确;
B.白磷在过量氢氧化钾溶液中反应生成KH2PO2,说明KH2PO2不与KOH反应,所以KH2PO2为正盐,由K+和H2PO![]() 构成,所以10.4 g该固体即
构成,所以10.4 g该固体即![]() =0.1mol该固体含离子数目为0.2NA,故B正确;
=0.1mol该固体含离子数目为0.2NA,故B正确;
C.根据题目所给反应可知反应过程P元素发生歧化反应,PH3为唯一还原产物,所以3molKOH参与反应时转移3mol电子,2.8gKOH即![]() =0.05molKOH参与反应时转移电子为0.05mol,即0.05NA,故C正确;
=0.05molKOH参与反应时转移电子为0.05mol,即0.05NA,故C正确;
D.KOH为强碱,所以室温下pH=11的KOH溶液稀释100倍后pH=9,则溶液中c(H+)=10-9mol/L,且氢离子全部由水电离,则水电离出的氢氧根也为10-9mol/L,溶液体积为10mL,所以n(OHˉ)=10-9mol/L×0.01L=10-11mol,故D错误;
故答案为D。

【题目】水浴加热滴加酚酞的NaHCO3溶液,颜色及pH随温度变化如下(忽略水的挥发):
时间 | ① | ② | ③ | ④ | ⑤ |
温度/℃ | 20 | 30 | 40 | 从40℃冷却到20℃ | 沸水浴后冷却到20℃ |
颜色变化 | 红色略加深 | 红色接近① | 红色比③加深较多 | ||
pH | 8.31 | 8.29 | 8.26 | 8.31 | 9.20 |
下列说法不正确的是( )
A.NaHCO3溶液显碱性的原因:HCO3-+H2O![]() H2CO3+OH-
H2CO3+OH-
B.①→③的过程中,颜色加深的原因可能是HCO3-水解程度增大
C.①→③的过程中,pH略微下降说明升温过程中c(OH-)减小
D.⑤比①pH增大,推测是由于NaHCO3分解生成的Na2CO3的缘故
【题目】氮的化合物在工业生产和生活中都有重要的应用,运用化学原理研究氮的单质及其化合物具有重要意义。
Ⅰ.一定条件下(T ℃、1.01×105 Pa),可以用Cl2(g)和NH3(g)制得NH2Cl(g),同时得到HCl(g)。已知部分化学键的键能如下表:
化学键 | N-H | Cl-Cl | N-Cl | H-Cl |
键能/kJ/mol | 391.3 | 243.0 | 191.2 | 431.8 |
写出该反应的热化学方程式:___________________________________________。
Ⅱ.亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在一定条件下合成:2NO(g)+Cl2(g) ![]() 2NOCl(g) ΔH<0。保持恒温恒容条件,将物质的量之和为3 mol的NO和Cl2以不同的氮氯比
2NOCl(g) ΔH<0。保持恒温恒容条件,将物质的量之和为3 mol的NO和Cl2以不同的氮氯比![]() 进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
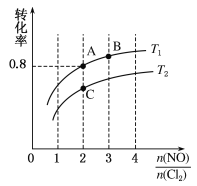
(1)图中T1、T2的关系为T1________T2(填“>”“<”或“=”)。
(2)图中纵坐标为物质________的转化率,理由为_________________________________。
(3)图中A、B、C三点对应的NOCl体积分数最大的是________(填“A”“B”或“C”)。
(4)若容器容积为1 L,经过10min到达A点,该时间段内化学反应速率υ(NO)=_________。B点的平衡常数为________。
(5)若在温度为T1,容积为1 L的容器中,充入0.5mol NO、1mol Cl2、2mol NOCl,υ(正)_____υ(逆) (填“<”“>”或“=”),理由为________________________________
【题目】氧、硫形成的化合物种类繁多,日常生活中应用广泛。如硫代硫酸钠(Na2S2O3)可作为照相业的定影剂,反应的化学方程式如下:AgBr+2Na2S2O3===Na3[Ag(S2O3)2]+NaBr。回答下列问题:
(1)基态S的价电子排布图为____________。
(2)下列关于物质结构与性质的说法,正确的是________。
A.玻尔原子结构模型能够成功地解释各种原子光谱
B.Br、S、O三种元素的电负性顺序为 O>Br>S
C.Na的第一电离能小于 Mg,但其第二电离能却远大于 Mg
D.水分子间存在氢键,故H2O的熔沸点及稳定性均大于H2S
(3)依据VSEPR理论推测![]() 的空间构型为______,中心原子S的杂化方式为________,[Ag(S2O3)2]3-中存在的化学键有________(填字母)。
的空间构型为______,中心原子S的杂化方式为________,[Ag(S2O3)2]3-中存在的化学键有________(填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键
(4)第一电子亲和能(E1)是指元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量(单位为kJ·mol-1),电子亲和能越大,该元素原子越易得电子。已知第三周期部分元素第一电子亲和能如下表:
元素 | Al | Si | P | S | Cl |
E1/(kJ·mol-1) | 42.5 | 134 | 72.0 | 200 | 349 |
表中元素的E1自左而右呈增大趋势,试分析P元素呈现异常的原因___________。
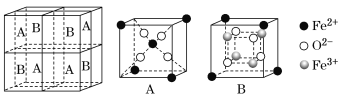
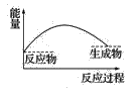
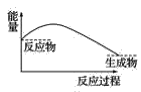
(5)某种离子型铁的氧化物晶胞如图所示,它由A、B组成。则该氧化物的化学式为_____,已知该晶体的晶胞参数为a nm,阿伏加德罗常数的值为NA,则密度ρ为______g·cm-3(用含a和NA 的代数式表示)。