题目内容
【题目】为了探究化学能与热能的转化,某实验小组设计了如下图所示三套实验装置: 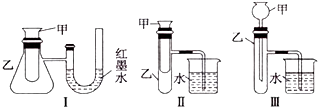
(1)图示3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是 .
(2)某同学选用装置I进行实验(实验前U形管里液面左右相平),在甲试管里先加入适量氢氧化钡溶再加入稀硫酸,U形管中可观察到的现象 , 说明该反应属于(填‘吸热”或“放热”)反应.
(3)为探究固体M遇水的热效应,选择装罝Ⅱ进行实验,先在甲中放入适量的水,再加入M. ①若M为钠,则实验过程中烧杯中可观察到的现象是 .
②若只观察到烧杯里的玻璃管内形成一段水柱,则M可能是 .
【答案】
(1)Ⅲ
(2)左端液柱降低,右端液柱升高;放热
(3)产生气泡,反应完毕后,冷却至室温,烧杯里的导管内形成一段水柱;硝酸铵
【解析】解:(1)装置Ⅰ可通过U形管中红墨水液面的变化判断铜与浓硝酸的反应是放热还是吸热;装置Ⅱ可通过烧杯中是否产生气泡判断铜与浓硝酸的反应放热还是吸热;装置Ⅲ只是一个铜与浓硝酸反应并将生成的气体用水吸收的装置,不能证明该反应是放热反应还是吸热反应, 所以答案是:Ⅲ;(2)氢氧化钡与硫酸反应属于中和反应,中和反应都是放热反应,所以锥形瓶中气体受热膨胀,导致U型管左端液柱降低,右端液柱升高,
所以答案是:左端液柱降低,右端液柱升高;放热;(3)①若M为钠,钠与水反应生成氢氧化钠和氢气,该反应为放热反应,放热的热量使大试管中温度升高,气体压强增大,所以右边烧杯中有气泡产生,反应完毕后,冷却至室温,烧杯里的导管内形成一段水柱,
所以答案是:产生气泡,反应完毕后,冷却至室温,烧杯里的导管内形成一段水柱;②若观察到烧杯里的玻璃管内形成一段水柱,说明M溶于水后导致大试管中温度降低,压强减小,证明M溶于水为吸热过程,溶于水能够吸收热量的物质有:硝酸铵、氯化铵等,
所以答案是:硝酸铵;

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】某同学完成如下探究实验:
实验目的:比较Cl2、Br2、I2三种单质的氧化性强弱
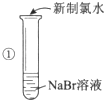
实验药品:NaBr溶液、KI溶液、氯水、淀粉溶液
实验记录:
实验步骤 | 实验现象 | 实验结论 |
| 溶液变为黄色 | 氧化性:Cl2>Br2 |
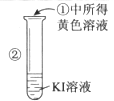
| 溶液变为黄色 | 氧化性: |
| 溶液的颜色由黄色变为蓝色 |
反思与评价:
(1)步骤①反应的离子方程式为: .
(2)检验②中所得黄色溶液含I2的另一种方法是(简述实验操作和相应的实验现象)
.
(3)你认为上述实验设计(填“能”或“不能”)达到实验目的,理由是 .