题目内容
【题目】由两种元素组成的化合物M,是某种具有优异磁学性质的新型电子材料的主要成分。其制备流程如下:

取2.38g 的M 用足量稀硫酸溶解,在所得反应液中加入足量的NaOH溶液,发现有刺激性气味且能使湿润红色石蕊试纸变蓝的气体产生,同时溶液中产生白色沉淀,迅速变成灰绿色,最终变为红褐色,沉淀灼烧后质量为3.20g。请回答:
(1)写出NaNH2的电子式________, M的化学式________________;
(2)根据图示信息,用一个化学方程式表示NaN3制备方法_________________________。
【答案】 ![]() Fe4N 2NaNH2+N2O=NaN3+NH3+NaOH
Fe4N 2NaNH2+N2O=NaN3+NH3+NaOH
【解析】根据流程可知,钠与氨气反应生成氨基钠和氢气,氨基钠进一步与一氧化二氮反应生成Na3N和氮气及氢氧化钠,M用足量稀硫酸溶解,在所得反应液中加入足量的NaOH溶液,发现有刺激性气味且能使湿润红色石蕊试纸变蓝的气体产生,说明有氨气产生,同时溶液中产生白色沉淀,迅速变成灰绿色,最终变为红褐色,说明白色沉淀为氢氧化亚铁,沉淀灼烧后质量为3.20g的氧化铁,氧化铁的物质的量为![]() =0.02mol,根据元素守恒可知,钠与GCl2及Na3N反应生成M和氮气、氯化钠,所以G为铁元素,M是含有2种元素组成的化合物,M中含有铁元素和氮元素,其中氮元素的物质的量为
=0.02mol,根据元素守恒可知,钠与GCl2及Na3N反应生成M和氮气、氯化钠,所以G为铁元素,M是含有2种元素组成的化合物,M中含有铁元素和氮元素,其中氮元素的物质的量为![]() =0.01mol,所以M中铁元素的氮元素的物质的量之比为0.02×2:0.01=4:1,所以M的化学式Fe4N。
=0.01mol,所以M中铁元素的氮元素的物质的量之比为0.02×2:0.01=4:1,所以M的化学式Fe4N。
(1)NaNH2为离子化合物,电子式为![]() ,根据上面的分析可知,元素G的名称为铁,M的化学式为Fe4N,故答案为:
,根据上面的分析可知,元素G的名称为铁,M的化学式为Fe4N,故答案为:![]() ;Fe4N;
;Fe4N;
(2)根据上面的分析可知,NaN3制备的方程式为2 NaNH2+N2O=NaN3+NH3+NaOH,故答案为:2 NaNH2+N2O=NaN3+NH3+NaOH;

【题目】I.大气中CO2含量的增多会导致地球表面温度升高及海洋生态环境改变。
已知:CO2(g)+CaO(s)![]() CaCO3 (s)
CaCO3 (s)
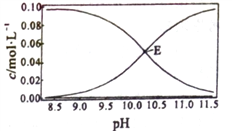
(1) 某研究小组在实验室探究不同温度对CaO吸收CO2效率的影响。在体积相同的密闭容器中,均充入一定量的生石灰和足量CO2,在不同温度下,保持其它初始实验条件不变,发生如上平衡分别在t秒时测定CO2的浓度(mol/L) 如图。

①该反应在__________条件下能自发进行。
A.较高温度 B.较低温度 C.任何温度 D.任何温度下均不能
②A、B、C、D、E五点中,达到化学平衡状态的点是_____________。
(2)在恒定温度下,一个体积固定为1L的容器中加入20gCaO和一定量的CO2气体,在10分钟达平衡的过程中CO2浓度变化如图所示,为提高CO2的吸收率,下列可以采取的措施有__________。
A.缩小反应容器的容积 B.升高温度
C.平衡体系中及时分离出部分CaCO3 D.使用合适的催化剂
若保持平衡时的温度不变,15分钟时将体积迅速增大至2L,在20分钟时重新达到平衡,请在下图中补充体积变化后CO2浓度变化示意图_______。

Ⅱ.在容积可变的密闭容器中发生反应:mA(g)+nB(g)![]() pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表
pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表
压强p/Pa | 2×105 | 5×105 | 1×106 |
c(A)mol·L-1 | 0.08 | 0.20 | 0.44 |
(3)当压强为1×106Pa时,此反应的平衡常数表达式:_________________________。
(4)电浮选凝聚法是工业上采用的一种污水处理方法,右图是该方法处理污水的实验装置示意图,实验过程中,污水的pH始终保持在5.0-6.0之间。接通电源后,阴极产生的气体将污物带到水面形成浮渣而刮去,起到浮选净化作用;阳极产生的沉淀具有吸附性,吸附污物而沉积,起到凝聚净化作用。

阳极区生成沉淀的总电极反应为:___________________________________。