题目内容
【题目】铋(Bi)及其化合物广泛应用于电子、医药等领域。一种以含铋矿石辉铋矿(主要成分为Bi2S3,含少量杂质PbO2等)为原料,采用湿法冶金制备铋单质的工艺流程如下:
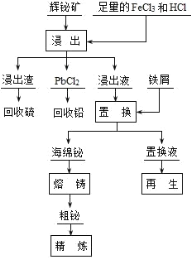
已知:PbCl2是一种难溶于冷水,易溶于热水的白色固体。 回答下列问题:
(1)铋(Bi)位于ⅤA族,铋的氢化物的热稳定性______氨气(填“大于”或“小于”)。
(2)“浸出”时,为了提高浸出速率,可采用的措施有______(任写一条)
(3)加热浸出时,PbO2 生成 PbCl2 和一种气体,此反应的化学方程式为______, 从产物中分离回收 PbCl2 的步骤是______、洗涤、干燥。从保护环境和原料循环利 用的角度,请指出上述工艺流程中可以采取的措施为______。
(4)电解精炼粗铋时必须补充含 Bi3+浓度高的电解液。可用粗铋、铅条作为两个电极,铅条外用素烧 的陶瓷坩埚作隔膜(Bi3+不能透过,H+能透过),电解液开始时为盐酸和食盐的混合液。则粗铋为电解池的 ______极,电解总反应为______。
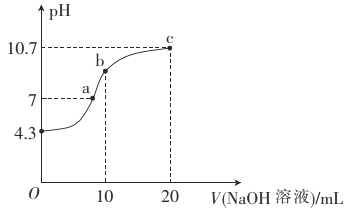
(5)25℃时,向浓度均为 0.02mol·L-1 的 Cu2+、Bi3+的混合溶液中滴加 Na2S 溶液(设溶液体积增加 1倍),使 Cu2+恰好沉淀完全即溶液中 c(Cu2+)=1×10-5 mol·L-1,此时是否有 Bi2S3 沉淀生成______(列式计算说明)。(已知:25℃时,Ksp(CuS)=6.0×10-36、Ksp(Bi2S3)=1.8×10-99)
【答案】小于 粉碎矿石、搅拌、适当提高浸取液温度 、适当提高溶液浓度等 PbO2 +4HCl![]() PbCl2 + Cl2↑+2H2O 冷却、过滤 “浸出”时生成的氯气,通入置换液中生成三氯化铁循环利用 阳
PbCl2 + Cl2↑+2H2O 冷却、过滤 “浸出”时生成的氯气,通入置换液中生成三氯化铁循环利用 阳  Qc(Bi2S3)=(0.01)2×(6.0×10-36÷1×10-5)3=2.16×10-95> Ksp(Bi2S3)= 1.8×10-99,故有Bi2S3沉淀生成
Qc(Bi2S3)=(0.01)2×(6.0×10-36÷1×10-5)3=2.16×10-95> Ksp(Bi2S3)= 1.8×10-99,故有Bi2S3沉淀生成
【解析】
辉铋矿(主要成分是Bi2S3、还含PbO2杂质)制备铋酸钠,辉铋矿加入氯化铁溶液和盐酸溶解后过滤,氯化铁氧化硫离子为硫单质:Bi2S3+6FeCl3=2BiCl3+6FeCl2+3S,盐酸是防止FeCl3及BiCl3水解生成不溶性沉淀,所以得到滤渣为S,滤液中含有Bi3+,H+,Pb2+,滤液冷却结晶可以得到PbCl2,然后回收铅;再次过滤得到的滤液中加入铁粉过滤得到海绵铋,置换液主要是氯化亚铁;对海绵铋进行熔铸、精炼得到金属铋;置换液中再通入氯气得到氯化铁溶液可以循环使用。
(1)同周期,从上往下,氢化物的稳定性逐渐降低,故铋的氢化物的热稳定性小于氨气;
(2)为了提高浸出率,可采取的措施有将矿石粉粹、搅拌,以增大接触面接,也可适当增大氯化铁溶液的浓度、适当升高温度等;
(3)浸出时,PbO2 生成PbCl2,Pb的化合价降低,则浸出液中HCl化合价升高生成Cl2,化学方程式为PbO2+4HCl=PbCl2+Cl2↑+2H2O;由于PbCl2难溶于冷水,易溶于热水,可对滤液进行冷却结晶然后过滤分离回收PbCl2;置换液为FeCl2,可将浸出时产生的Cl2通入置换液中,使FeCl2转化为FeCl3循环利用,同时防止污染环境;
(4)电解时金属铋需要被氧化生成Bi3+,电极池中阳极得电子发生氧化反应,所以粗铋为电解池的阳极;阴极得电子发生还原反应,根据电解质溶液中的离子种类可知阴极应是氢离子得电子生成氢气,所以电解总反应为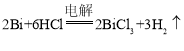 ;
;
(5)Cu2+恰好沉淀完全即溶液中c(Cu2+)=1×10-5molL-1,则此时溶液中c(S2-)=![]() ,此时Qc(Bi2S3)=0.012×(
,此时Qc(Bi2S3)=0.012×(![]() )3=2.16×10-95>Ksp(Bi2S3)=1.8×-99,故有Bi2S3沉淀生成。
)3=2.16×10-95>Ksp(Bi2S3)=1.8×-99,故有Bi2S3沉淀生成。

 小题狂做系列答案
小题狂做系列答案